Los intrones son segmentos de ADN presentes en la transcripción primaria de ARN que, a diferencia de los exones (secuencias codificantes), son eliminados del transcrito maduro mediante un proceso conocido como splicing antes de su traducción. La palabra "intrón" proviene del término "región intragénica", indicando una secuencia localizada dentro de un gen.
Los intrones fueron descubiertos independientemente en 1977 por Phillip Allen Sharp y Richard J. Roberts, un hallazgo que les valió el Premio Nobel de Fisiología o Medicina en 1993. Posteriormente, Thomas R. Cech y Sidney Altman recibieron el Premio Nobel de Química por el descubrimiento de que algunos intrones (del grupo I y II) son ribozimas, es decir, moléculas de ARN con actividad catalítica capaz de realizar su propio autoempalme.
Clasificación y Funciones de los Intrones
El número y la longitud de los intrones varían considerablemente entre diferentes especies y entre los genes de un mismo organismo. Tradicionalmente se creía que los intrones eran fragmentos de ADN carentes de información, una afirmación que hoy en día es ampliamente cuestionada. Se ha demostrado que, aunque no codifican productos proteicos directamente, son parte integral de la regulación de la expresión génica.
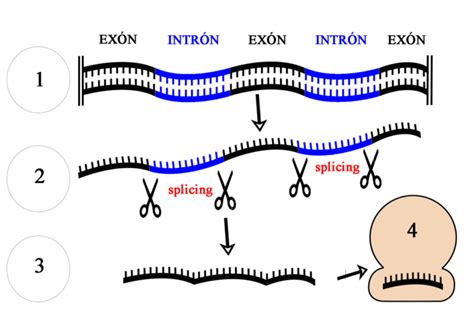
Los intrones se clasifican según su mecanismo de empalme:
- Los intrones del grupo I, II y III son intrones autocatalíticos que sufren autoempalme mediante reacciones de transesterificación. Los intrones del grupo II y III son muy similares y presentan una estructura secundaria altamente conservada; de hecho, a veces los intrones del grupo III son identificados como intrones del grupo II. Los intrones del grupo I están presentes en los genes de ARNr de algunos eucariotas inferiores y en los genes mitocondriales de hongos.
- Los intrones del grupo II y III se eliminan mediante un proceso autocatalítico que requiere una adenina o un espliceosoma, respectivamente.
- Los intrones espliceosomales son los más comunes en eucariotas superiores y se eliminan por el espliceosoma, un complejo molecular.
Además de su papel en el procesamiento del ARN, los intrones cumplen otras funciones vitales:
- Pueden actuar como sitios alternativos de empalme, lo que permite generar múltiples tipos de proteínas a partir de un solo gen (empalme alternativo), aumentando la variabilidad funcional.
- Algunos intrones codifican ARN funcionales a través de un procesamiento adicional después del empalme, generando moléculas de ARN no codificantes.
- Contribuyen a la estabilidad genómica: en genes de levadura altamente expresados, los intrones inhiben la formación de bucles R (estructuras vulnerables al daño del ADN) y disminuyen el daño al ADN en comparación con genes sin intrones de expresión similar. La inserción de un intrón dentro de un gen propenso a bucles R puede suprimir su formación y recombinación.
Evolución de los Intrones: Ganancia y Pérdida
La estructura intrón-exón de genes homólogos puede variar ampliamente entre diferentes organismos. Estudios recientes han demostrado que la longitud y la densidad de los intrones (intrones/gen) varían considerablemente incluso entre especies relacionadas. Por ejemplo, el genoma humano contiene una media de 8.4 intrones/gen, mientras que el hongo unicelular Encephalitozoon cuniculi solo tiene 0.0075 intrones/gen. Se cree que este proceso está sujeto a selección, con una tendencia hacia la ganancia de intrones en especies más grandes y la pérdida en especies más pequeñas (particularmente unicelulares).
Existen dos modelos contrapuestos sobre el origen y la evolución de los intrones nucleares: el modelo de intrones tempranos (IE), que propone que los intrones eran muy numerosos en los ancestros de procariotas y eucariotas y se fueron perdiendo, y el modelo de intrones tardíos (IL), que sugiere que los intrones aparecieron tras la divergencia de procariotas y eucariotas.
A lo largo del tiempo evolutivo, los intrones pueden perderse o ganarse, como lo demuestran numerosos estudios comparativos de genes ortólogos. Se han identificado dos mecanismos definitivos de pérdida de intrones: la pérdida de intrones mediada por transcriptasa inversa (RTMIL) y las deleciones genómicas. Sin embargo, los mecanismos exactos de la ganancia de intrones son más complejos y controvertidos, habiéndose informado al menos siete mecanismos:
- Transposición de intrones: Un intrón empalmado invierte el empalme en su propio ARNm o en otro ARNm en una posición previamente sin intrones. Este ARNm que contiene intrones se transcribe de forma inversa, y el ADNc resultante puede provocar una ganancia de intrones mediante recombinación con su locus genómico original.
- Inserción de transposones: La inserción de transposones puede intronizar el elemento sin interrumpir la secuencia codificante si se inserta en una secuencia AGGT.
- Duplicación genómica en tándem: Una duplicación en tándem intragénica corta puede insertar un intrón nuevo en un gen codificador de proteínas, dejando la secuencia peptídica correspondiente sin cambios. Esta es el único mecanismo propuesto con pruebas experimentales in vivo de respaldo.
- Transferencia de intrones: Un parálogo o un pseudogen gana un intrón y lo transfiere a una ubicación sin intrones en su parálogo hermano mediante recombinación.
- Ganancia de intrones durante la reparación de roturas de doble cadena (DSBR): Identificada recientemente como una fuente de ganancia de intrones, asociada a repeticiones directas cortas que flanquean intrones.
- Inserción de un intrón del grupo II.
- Intronización: Mutaciones crean nuevos intrones a partir de una secuencia anteriormente exónica, sin necesidad de inserción de ADN.
Intrones en Levaduras: El Caso de Saccharomyces cerevisiae
La levadura de gemación Saccharomyces cerevisiae, también conocida como levadura de pan o cerveza, es uno de los organismos modelo más empleados en investigación biomédica y evolutiva. Sus ventajas incluyen una rápida división celular (aproximadamente 2 horas), facilidad de cultivo en laboratorio y un genoma pequeño y ampliamente conocido de alrededor de 6000 genes. Una característica notable de su genoma es que prácticamente no presenta intrones, lo que simplifica el estudio genético.
A pesar de su escasez, los intrones presentes en S. cerevisiae desempeñan funciones importantes. El genoma de la levadura de la cerveza solo tiene 295 intrones en 280 genes (hay 9 genes con más de un intrón). Investigaciones han demostrado que estos intrones están implicados en la regulación del crecimiento celular. Un estudio detallado indica que los intrones reprimen la expresión de ciertos genes de proteínas ribosomales implicadas en las rutas metabólicas de la proteína quinasa TORC1 y la proteína quinasa PKA, que son cruciales para la detección de nutrientes.
Un estudio publicado en Nature (Parenteau et al., 2019) reveló que los intrones espliceosomales en S. cerevisiae, en condiciones de inanición, no se degradan tras su transcripción, sino que regulan el crecimiento celular. Usando técnicas de edición génica CRISPR-Cas9, se confirmó la hipótesis de que estos intrones reprimen las rutas metabólicas de TORC1 y PKA, influyendo en la respuesta celular al estrés ambiental. El plegamiento del ARN transcrito es también un factor clave en la función de estos intrones.
CICLO CELULAR Y SUS FASES | Interfase y Mitosis
Contexto Genómico y Evolutivo de Saccharomyces cerevisiae
Durante su evolución, el genoma de S. cerevisiae se ha modificado constantemente. Un evento destacado es la duplicación del genoma completo (WGD), que ocurrió hace aproximadamente 100 millones de años. Este evento supuso que el genoma de un ancestro común de Saccharomyces y otros géneros de levaduras se duplicara, dando lugar a una célula tetraploide. Posteriormente, se produjo una pérdida de muchos de los genes duplicados y una reordenación cromosómica, conservándose hasta un 13% de los genes duplicados.
Los efectos más relevantes de esta duplicación incluyen un flujo glucolítico aumentado, gracias a la conservación de copias duplicadas de genes relacionados con la glicólisis (como los genes ADH1 y ADH2), y la aparición de la estrategia MAC (make-accumulate-consume). Esta estrategia permite a S. cerevisiae utilizar rápidamente la glucosa durante la fermentación produciendo etanol (make), mantener el metabolismo fermentativo para producir etanol independientemente de la presencia de oxígeno (accumulate) y una posterior utilización del etanol como fuente de carbono (consume).
Investigadores del Centro de Regulación Genómica (CRG), liderados por Marina Marcet-Houben y Toni Gabaldón, propusieron una nueva teoría sobre el origen de esta duplicación del genoma. Sus resultados, publicados en PLOS Biology, demuestran que la aparición de genes duplicados no fue causada por una simple duplicación del genoma entero, sino que fue fruto de la hibridación entre dos especies diferentes. Utilizando metodología computacional de última generación, reconstruyeron duplicaciones de genes y determinaron que la edad de los genes duplicados era mucho mayor de lo que predecía la teoría de la duplicación simple del genoma, lo que apoyó la hipótesis de hibridación.
Esta hipótesis tiene grandes implicaciones sobre cómo se interpreta el origen y la evolución de los genomas duplicados, sugiriendo que no son necesarios cambios masivos y rápidos para originar nuevas funciones a partir de secuencias duplicadas. La propuesta se ve reforzada por la observación de un mayor número de duplicaciones de genoma en plantas cultivadas, lo que podría indicar situaciones evolutivas similares.
Intrones Mitocondriales y Caracterización de Cepas
En cada célula haploide de S. cerevisiae existen aproximadamente de 50 a 200 copias de ADN mitocondrial, que corresponde al 15% del ADN total celular. Este ADN está compuesto principalmente por fragmentos lineales de 75 a 150 kb, aunque también se encuentran moléculas circulares. El ADN mitocondrial de S. cerevisiae se caracteriza por un bajo contenido de GC y regiones intergénicas extensas ricas en adenina y timina.
A pesar de su importancia, mutaciones que afectan la fosforilación oxidativa (fenotipo petite) o incluso la pérdida total del genoma mitocondrial (fenotipo rho0) no son letales para S. cerevisiae, aunque comprometen la supervivencia a temperaturas extremas o afectan la tolerancia al etanol. La herencia mitocondrial tiene un gran impacto en la resistencia al estrés oxidativo y a la deshidratación, procesos relevantes en la industria vitivinícola.
Un método de PCR basado en las variaciones en el número y posición de intrones en el gen mitocondrial COX1 entre distintas cepas de S. cerevisiae se ha propuesto para diferenciar cepas, con la ventaja de no requerir la purificación de ADN genómico. Esto subraya la importancia de los intrones, incluso los mitocondriales, en la identificación y estudio de la diversidad de levaduras.