La visualización de estructuras celulares microscópicas, ya sean en tejidos animales, vegetales o microorganismos, frecuentemente requiere el uso de colorantes específicos. Así como para observar tejidos animales es imprescindible usar colorantes que diferencien el núcleo del citoplasma, en el caso de los tejidos y órganos vegetales se utilizan colorantes con afinidad por las paredes celulares.
La safranina es un colorante comúnmente empleado en diversas aplicaciones histológicas y microbiológicas. Se conoce que la safranina O tiñe de rojo intenso el nucleolo, aunque no reacciona con otros componentes nucleares, una propiedad útil para la identificación de ciertas estructuras. Su aplicación varía según el tipo de muestra y el objetivo de la tinción.
Procedimientos de Tinción con Safranina en Tejidos Vegetales
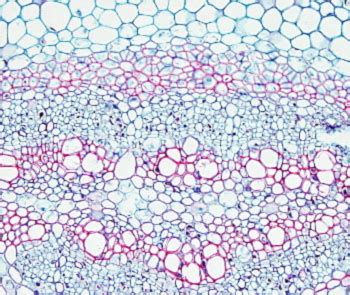
Para la observación de tejidos vegetales, se parte de muestras fijadas con FAA (formaldehído, alcohol, acético) y cortadas en vibratomo o en microtomo de congelación, o de cortes de inclusiones en parafina. Los cortes gruesos tendrán un grosor mínimo de 40-50 μm y se manipulan con pincel, realizando los pasos en los diversos líquidos en pocillos pequeños con volúmenes reducidos. Los cortes de parafina se procesan de manera convencional.
Protocolo de Tinción con Safranina y Azul Alcián
Un procedimiento común para la tinción de tejidos vegetales utiliza safranina en combinación con azul alcián:
- Etanol de 50°.
- Tinción en safranina.
- H2O destilada.
- Tinción en azul alcián (1 %, pH 2.5). Se recomienda poner en agitación al menos una hora y posteriormente filtrar.
- H2O destilada.
- Diferenciar con alcohol de 96° hasta que la mayor parte del tejido adquiera color azul claro.
- Etanol 100°.
- Xileno.
Protocolo de Tinción con Safranina y Verde Rápido
Otro protocolo para cortes histológicos vegetales implica el uso de safranina y verde rápido:
- Etanol de 50°.
- Tinción en safranina (1 %, pH 2.5).
- H2O destilada.
- Etanol 96°.
- Tinción en verde rápido (1%) durante 60 segundos.
- Etanol 100°.
- Xileno.
Generalmente, el protocolo rápido para obtención de cortes histológicos vegetales supone el uso de vibratomo o micrótomo de congelación. Sin embargo, se pueden obtener buenas tinciones y calidad del tejido con inclusión en parafina y cortes por debajo de las 10 µm.
Uso de Safranina en la Tinción Nuclear de Hongos
Para la caracterización de especies de hongos en función de su número de núcleos (uni, bi o multinucleadas), se han desarrollado varios métodos de tinción nuclear. Entre los colorantes utilizados se encuentran la acridina naranja, azules de anilina y tripano, diamina fenil indol (DAPI), Giemsa, hematoxilina, orceína y safranina O. Varios de estos procedimientos, incluyendo la safranina O, han sido catalogados como rápidos.
La safranina O tiene la particularidad de teñir de rojo intenso el nucleolo, pero no reacciona con los otros componentes nucleares. Sin embargo, en algunas aplicaciones, como la observación nítida e integral de núcleos y nucleolos en hongos del complejo Rhizoctonia, la safranina O y otros colorantes rápidos pueden generar dudas sobre la identidad de las estructuras teñidas, ya que existe la probabilidad de contabilizar como núcleos a vacuolas cargadas con afinidad por estos colorantes. En este contexto, un método alternativo que proporciona imágenes más claras de las estructuras nucleares utiliza fucsina ácida al 0,025 % en ácido láctico al 50 %.
Safranina en Sistemas de Análisis Automatizados
En el ámbito del análisis automatizado de partículas, especialmente para células sanguíneas, la safranina O forma parte de composiciones de agentes de contraste. Una composición de agentes de contraste de partículas puede incluir al menos dos agentes seleccionados del grupo que consiste en cristal violeta, nuevo azul de metileno, eosina Y y safranina O. Estas composiciones suelen incluir un agente de permeabilización como la saponina, en cantidades suficientes para generar concentraciones específicas en las condiciones de tinción, y pueden optimizarse para sistemas de citometría de flujo automatizados.
Saccharomyces cerevisiae: Aislamiento, Selección e Identificación (Métodos Sin Safranina)
Aunque la safranina es un colorante comúnmente empleado en diversas aplicaciones histológicas y microbiológicas, los procedimientos detallados proporcionados para el aislamiento y la identificación de levaduras Saccharomyces en este contexto se basan en metodologías específicas que no incluyen la tinción con safranina, sino otras técnicas como medios selectivos y análisis moleculares para la caracterización enológica.
Contexto Enológico de Saccharomyces spp. en Querétaro
Querétaro es el segundo estado productor de vinos en México, enfrentando desafíos en la comercialización debido a la falta de calidad y tipicidad. Una alternativa para mejorar esta situación es la selección de levaduras nativas que puedan aumentar el potencial de los mostos y conferir originalidad a los vinos. La calidad del vino se fundamenta en el aspecto sensorial, vinculado a los compuestos químicos presentes y su equilibrio para una experiencia organoléptica agradable. Se han establecido rangos aceptables de concentración para compuestos clave como etanol, acidez volátil y SO2, así como recomendaciones para azúcares residuales y acidez total.
En la elaboración de vinos, la fermentación alcohólica (FA) es una etapa fundamental, donde las levaduras, como el género Saccharomyces, convierten los azúcares en etanol. El género Saccharomyces destaca por su alta eficiencia en la conversión de azúcares y su tolerancia a concentraciones elevadas de etanol y SO2, siendo el género fermentativo por excelencia.
Formas de Fermentación Alcohólica
La FA puede ocurrir de tres maneras:
- Espontánea: Utiliza la microbiota natural presente en el epicarpio de la uva o en las superficies de la bodega, realzando la tipicidad del vino con características únicas de los microorganismos nativos.
- Adición de Levadura Seca Activa (LSA): Proporciona un proceso reproducible y controlable, aunque puede restar tipicidad al producto.
- Inoculación con Levaduras Nativas Seleccionadas: Permite procesos controlables y reproducibles, manteniendo el carácter único y típico que los microorganismos nativos proporcionan.
Los criterios para seleccionar cepas de levaduras enológicas incluyen buena eficiencia fermentativa, baja producción de SO2 y H2S, resistencia al factor killer o su presencia, y tolerancia a altos niveles de etanol y SO2. Es importante considerar necesidades regionales específicas, como la adaptación a bajas temperaturas, la producción de aromas o el uso de mostos con altas concentraciones de azúcares.
Metodología para Aislamiento y Caracterización de Saccharomyces
Material Biológico y Sitios de Estudio
En un estudio específico, se utilizaron frutos de vid (Vitis vinifera) de los cultivares Merlot y Cabernet Sauvignon, cosechados en madurez fisiológica aparente durante 2012 en tres viñedos comerciales en el estado de Querétaro. La ubicación geográfica de estos viñedos incluyó El Rosario (El Marqués), El Barreno (San Juan del Río) y Viñedos Azteca (Ezequiel Montes).
Aislamiento y Diferenciación de Cepas Saccharomyces
Los frutos recolectados al azar fueron llevados a laboratorio para estrujarlos y fermentarlos espontáneamente en bolsas plásticas estériles a 25 °C durante 8 días. Cada 2 días, se tomaron alícuotas para realizar diluciones decimales y sembrar en agar papa dextrosa (APD) con rosa de Bengala y ampicilina, incubándose 5 días a 25 °C. Las colonias con morfología típica de levaduras se sembraron en medio Agar Nutritivo-Dextrosa para levaduras (NYDA) e incubaron 3 días a 25 °C. Para diferenciar las cepas del género Saccharomyces, las levaduras aisladas se sembraron en dos pases consecutivos en medio agar Lisina, que es selectivo para no-Saccharomyces, incubándose 4 días a 25 °C.
Evaluación de Tolerancia (SO2 y Etanol)
Se colocó una concentración de 6 Log de UFC de cada levadura en pozos individuales con caldo nutritivo-dextrosa para levaduras (NYDB) ajustado a pH 3.5 y 25 °Brix, en presencia de etanol (12 %) o SO2 (200 mg L-1). La viabilidad se verificó inoculando en el mismo medio NYDB sin los compuestos a evaluar. Las variables cinéticas evaluadas fueron el tiempo de detección (h), que indica la duración de la fase de adaptación (tiempos más cortos suponen mayor tolerancia), y la velocidad de desarrollo, que representa el incremento de DO por unidad de tiempo (DO min-1).
Tolerancia al Fenotipo Killer
Para evaluar la tolerancia al fenotipo killer, la cepa de referencia K1 (killer) se incubó 72 horas a 25 °C en medio NYDB (pH 3.5). Posteriormente, el caldo de cultivo se filtró para separar las células de la cepa del caldo-toxina, el cual fue recuperado para ser probado en las cepas aisladas. El equipo se programó para realizar lecturas cada 20 minutos durante 72 horas a 25 °C y evaluar el máximo crecimiento de la levadura, determinando el porcentaje de inhibición.
Pruebas de Microvinificación
Las pruebas de microvinificación se realizaron con las levaduras seleccionadas previamente. Para eliminar microorganismos, las uvas despalilladas se sometieron a termovinificación (60 °C, 20 min). Posteriormente, las uvas se prensaron asépticamente para obtener mostos, ajustados a pH 3.5 y 25 °Brix. Las cepas de levaduras seleccionadas se incubaron 48 horas a 25 °C en medio NYDB, ajustándose a una concentración final en el mosto de 5 Log de UFC mL-1. La fermentación se realizó en matraces en condiciones estériles y de semianaerobiosis, controlando el peso cada 24 horas hasta que fue constante.
Variables Fermentativas y Físico-Químicas del Vino
El comportamiento fermentativo se determinó mediante las siguientes variables:
- Grado alcohólico, por destilación directa y picnometría.
- Eficiencia fermentativa, como porcentaje de alcohol producido respecto al grado alcohólico potencial.
- Conversión azúcar/etanol, en gramos de azúcar utilizados para producir un grado alcohólico.
- Velocidad de fermentación, expresada en gramos de CO2 desprendido cada 48 horas.
Además, se determinaron variables físicas y químicas de los vinos como:
- Azúcares reductores, por el método de Fehling Causse Bonnans.
- pH, usando un potenciómetro calibrado a dos puntos.
- Acidez total titulable (ATT) mediante titulación.
- Acidez volátil (AV) por el método de García-Tena.
- SO2 total, por el método de Rippert.
Ocho cepas destacaron por su tolerancia a SO2, etanol y fenotipo killer, incluyendo Saccharomyces cerevisiae (SR19, SR26, SR27, N05) y S. paradoxus (N42, SR25, OB10, OB11). Los vinos producidos con estas levaduras fueron secos, con acidez total de 6.5 a 8.4 g L-1 de ácido tartárico, acidez volátil de 0.13 a 0.26 g L-1 de ácido acético y pH de 3.56 a 3.74. Las cepas nativas N05 y K1 (testigo) obtuvieron los mayores grados alcohólicos (15.2 y 14.9 %) y eficiencias de conversión y fermentativa.
Identificación Molecular de las Levaduras (PCR)
Para la identificación de las levaduras, se empleó la técnica de PCR, amplificando el dominio D1/D2 del gen que codifica para la subunidad 26S del ARNr. La extracción de ADN se realizó mediante un protocolo que incluye calor y purificación con fenol-cloroformo. La reacción de PCR utilizó los oligonucleótidos universales NL1 y NL4 con condiciones específicas de temperatura y ciclos. Los productos obtenidos fueron enviados para secuenciación masiva de ADN.
tags: #levadura #s #cerevisiae #safranina