La gelatina es una mezcla de proteínas obtenida mediante la hidrólisis parcial del colágeno, extraída comúnmente de la piel, los huesos y los tejidos conectivos de animales como cerdos, vacas y peces. A temperatura ambiente, se presenta como un sólido inodoro e insípido, de color amarillo pálido a amarillo. Su propiedad más distintiva es la gelificación termorreversible: se disuelve en agua caliente y forma un gel al enfriarse, volviendo a fundirse al calentarse. Como un importante material polimérico natural, la gelatina se utiliza ampliamente en la industria alimentaria, farmacéutica y en productos industriales debido a su buena biocompatibilidad, degradabilidad y multifuncionalidad.
La gelatina ha sido la columna vertebral de las industrias farmacéutica y de suplementos dietéticos durante más de un siglo, reconocida por su fiabilidad y seguridad como excipiente de cubierta. Fue inventada en 1834 por el farmacéutico francés F. A. B. Mothes, y a finales del siglo XIX, Estados Unidos se convirtió en líder mundial en el desarrollo de cápsulas de gelatina.
Tipos de Cápsulas de Gelatina
Las cápsulas de gelatina se presentan en dos formas principales para la administración oral de fármacos:
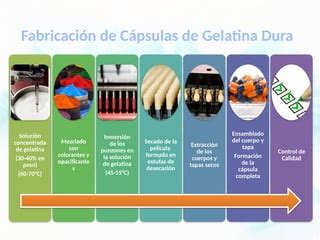
- Cápsulas duras: Son envolturas cilíndricas rígidas de dos partes (cuerpo y tapa) que se rellenan con ingredientes secos o líquidos y se sellan para evitar fugas. Representan el 75% del mercado de cápsulas de gelatina y pueden contener polvos, gránulos, pellets y tabletas diminutas.
- Cápsulas blandas (softgels): Son cápsulas de una sola pieza con una cubierta flexible, herméticamente cerradas, que se benefician de la capacidad de la gelatina para disolverse en agua caliente y formar un gel al enfriarse. Ofrecen ventajas como la protección de principios activos, mejora de la deglución y fácil disolución en los jugos gástricos.
Propiedades Fisicoquímicas y Reactividad Química de la Gelatina
Las propiedades fisicoquímicas de la gelatina están determinadas por su naturaleza proteica y su origen en el colágeno, siendo afectadas por las materias primas, el método de extracción (ácido para tipo A, alcalino para tipo B) y el proceso.
Gelificación Termorreversible
Esta es la propiedad más característica de la gelatina. Una solución caliente de gelatina forma un gel sólido al enfriarse por debajo de los 35-40°C, y se funde nuevamente al calentarse. Este proceso puede repetirse indefinidamente. El mecanismo de gelificación implica que durante el enfriamiento, las cadenas polipeptídicas de gelatina recuperan parcialmente su estructura de triple hélice y, mediante fuerzas como los enlaces de hidrógeno, forman una red tridimensional que atrapa las moléculas de agua, creando el gel.
La resistencia del gel (grado Bloom) es un indicador crítico de la calidad, reflejando la dureza y rigidez del gel. Depende principalmente del peso molecular promedio de la gelatina y de la proporción de componentes de alto peso molecular.
Solubilidad e Hinchamiento
La gelatina no es soluble en agua fría, pero puede absorber agua lentamente e hincharse. La gelatina hinchada se disuelve completamente al calentarse por encima de los 40-50°C, formando una solución coloidal viscosa. Además del agua caliente, es soluble en soluciones acuosas de polioles o ácidos orgánicos, pero no en la mayoría de los disolventes orgánicos.
Viscosidad
La viscosidad de una solución de gelatina es determinada por su concentración, temperatura, peso molecular y valor de pH. Un aumento de la concentración y el peso molecular incrementa la viscosidad, mientras que un aumento de la temperatura la disminuye. La viscosidad alcanza su valor mínimo cuando el pH de la solución se aproxima al punto isoeléctrico de la gelatina.
Anfólito y Punto Isoeléctrico
Las cadenas moleculares de la gelatina contienen grupos amino libres (-NH₂, básicos) y grupos carboxilo (-COOH, ácidos), lo que la convierte en un anfólito. La gelatina tipo A (método ácido) tiene un punto isoeléctrico más alto (pH 7.5-9.0), mientras que la gelatina tipo B (método alcalino) tiene un punto isoeléctrico más bajo (pH 4.8-5.0). Esta diferencia afecta directamente su solubilidad, viscosidad y comportamiento de gelificación.
Reactividad Química y Degradación
Los abundantes grupos funcionales (-NH₂, -COOH, -OH) en las cadenas de la gelatina le permiten participar en diversas reacciones químicas:
- Reacción de reticulación: Reacciona con aldehídos como formaldehído o glutaraldehído para formar una red estable e insoluble en agua. Esta reacción es crucial en la fabricación de cápsulas duras de gelatina y esponjas hemostáticas quirúrgicas, pero también es la causa principal de problemas de estabilidad.
- Reacciones de modificación: Mediante acilación, esterificación o copolimerización por injerto, se pueden alterar sus propiedades como el punto de fusión, resistencia mecánica o dotarla de nuevas funcionalidades.
La gelatina es sensible a la degradación, hidrolizándose en condiciones de ácidos fuertes, álcalis fuertes o alta temperatura, lo que provoca la ruptura de las cadenas moleculares y la pérdida de sus propiedades. Ciertas enzimas proteolíticas también pueden degradarla.
El Reto del Entrecruzamiento (Cross-linking) por Aldehídos en Cápsulas de Gelatina
A pesar de la versatilidad y el uso extensivo de la gelatina, los fabricantes de sistemas de administración de fármacos sólidos orales (OSD) enfrentan un desafío persistente: el entrecruzamiento (cross-linking) de la gelatina. Este fenómeno, observado inicialmente en 1974 para cápsulas duras con cloranfenicol, plantea una seria amenaza a la disolución de productos farmacéuticos.
Tras la ingestión, el objetivo principal de las cápsulas de gelatina es liberar su contenido. Sin embargo, con el envejecimiento, las formulaciones a base de gelatina pueden experimentar fallas de disolución debido a la reticulación en productos estresados. Este proceso provoca la formación de una membrana hinchada, delgada, dura, gomosa e insoluble en agua, conocida como "película".
Esta película actúa como una barrera para la liberación del fármaco, resultando en una liberación más lenta o nula en estudios in vitro. El grado de reticulación puede variar, dificultando la predicción del problema. Una vez formadas, estas películas son irreversibles y hacen que la gelatina sea insoluble, lo que lleva a una mayor variabilidad en los resultados de disolución. Esto puede llevar al incumplimiento de las directrices regulatorias y, en casos extremos, a la retirada del producto del mercado.
Investigaciones han descubierto que el endurecimiento de cápsulas de gelatina blanda con ácidos grasos poliinsaturados omega-3 se debe a una interacción química entre la formulación y la gelatina, lo que reduce el periodo de validez y puede afectar la eficacia del tratamiento si la liberación del fármaco ocurre más allá del intestino delgado. Sin embargo, una ventaja es que la velocidad de endurecimiento de la gelatina porcina (tipo A) es significativamente menor que la de la gelatina bovina (tipo B) en estas formulaciones, prolongando el periodo de validez y ofreciendo una alternativa a la gelatina de origen bovino, sobre la cual existen preocupaciones por la posible transmisión de encefalopatías espongiformes.
Mecanismo del Entrecruzamiento de la Gelatina
La gelatina, compuesta principalmente de aminoácidos unidos por enlaces amida, es susceptible al entrecruzamiento debido a interacciones químicas entre sus cadenas peptídicas o aminoácidos individuales. Estas interacciones pueden ser provocadas por pequeñas cantidades de aldehídos presentes en excipientes o ingredientes activos (API), por la descomposición de componentes de la formulación o materiales de empaque, o por la exposición a condiciones severas como altas temperaturas y humedad.
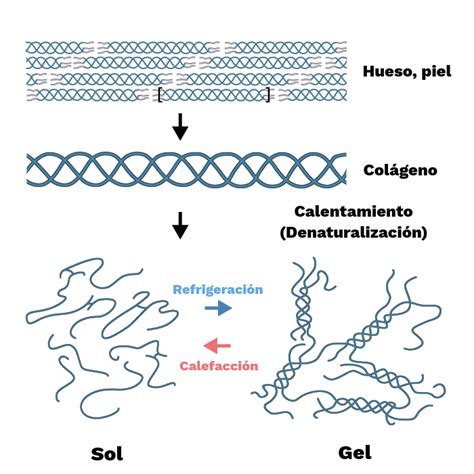
El entrecruzamiento en la gelatina puede ser de dos tipos:
- Reticulación interna: Ocurre cuando las cápsulas de gelatina se exponen a altas temperaturas y humedad, afectando principalmente sus superficies internas.
- Reticulación externa: Se produce cuando formulaciones a base de gelatina interactúan con sustancias como aldehídos, peróxidos o ácidos sulfónicos, provocando cambios químicos que transforman las moléculas de gelatina de una configuración de espiral aleatoria a una estructura de triple hélice de colágeno.
El mecanismo de entrecruzamiento implica tres vías principales:
- Entrecruzamiento intra e intercadenas: Surge de interacciones entre aminoácidos (especialmente lisina) dentro de la misma molécula de gelatina (intracadenas) o entre moléculas vecinas (intercadenas). Los residuos de lisina cercanos sufren desaminación oxidativa, generando grupos aldehído terminales que reaccionan con grupos ε-amino vecinos de lisina para formar intermediarios de imina. Las reacciones de condensación aldólica posteriores forman productos reticulados que contienen anillos de piridinio. Este proceso es catalizado por calor, humedad relativa o agentes químicos.
- Reacción con grupos carbonilo: Implica la interacción entre los grupos lisil ε-amino y las impurezas aldehídicas contaminantes, generando derivados de hidroximetilamino que se deshidratan para formar iminas. Estas iminas reaccionan con residuos de hidroximetil lisina, formando puentes de dimetil éter, y reordenamientos resultan en enlaces metileno entre grupos lisil ε-amino. Reacciones similares ocurren con azúcares aldosa, donde los intermediarios de imina reaccionan con grupos amino libres para producir azúcares cetosa, llevando al entrecruzamiento.
- Formación de aminales: El entrecruzamiento también puede ocurrir mediante la formación de aminales (aminas derivadas de acetales), proceso influenciado por el pH del medio ambiente.
Factores que Influyen en el Entrecruzamiento
Diversos factores ambientales y químicos pueden exacerbar la reticulación de la gelatina:
Factores Ambientales
- Humedad elevada: Facilita la catálisis directa de la formación de iminas. Ciertos excipientes pueden producir subproductos en ambientes húmedos (ej., el almidón de maíz descompone hexametil tetramina en amoníaco y formaldehído). También puede inducir la reticulación arginina-arginina.
- Temperaturas elevadas: Aceleran la velocidad de las reacciones de reticulación, acelerando la formación de redes de gelatina insolubles.
- Exposición a la luz o radiación UV: Puede influir en las propiedades de disolución, correlacionándose con una reducción en las tasas de disolución in vitro.
Factores Químicos
La Tabla 2 resume los principales agentes causantes de entrecruzamiento:
| Factor | Procesador | Agente Causante del Entrecruzamiento | Reacción Resultante |
|---|---|---|---|
| Humedad | Ligera | - | Implicada en formación de iminas y otros subproductos. |
| Excipientes o API con grupo funcional carbonilo | Aldehídos (furfural, acroleína, formaldehído, gliceril aldehído) y cetonas | Iminas | Formación de enlaces imina y puentes de dimetil éter. |
| Azúcares | Azúcares (glucosa y azúcar aldosa) | - | Reacciones con iminas y grupos amino libres. |
| Agente oxidante | PEG (que contienen peróxido/aldehídos) | - | Liberación de aldehídos de bajo peso molecular. |
| Iones metálicos | (colorantes/tintes) | - | Pueden catalizar reacciones de reticulación. |
| Polisacáridos sulfatados | (sulfato de condroitina) | - | Pueden interactuar con la gelatina. |
Un contribuyente destacado es el formaldehído, que puede liberarse de plastificantes, conservantes y compuestos polietilenados como el polietilenglicol (PEG), usado frecuentemente como disolvente. Los PEG pueden liberar aldehídos de bajo peso molecular bajo condiciones aeróbicas. Aldehídos como el furfural, encontrados en botellas con bobinas de rayón, también reaccionan con la gelatina formando productos reticulados insolubles.
Detección del Entrecruzamiento
Se han aplicado técnicas instrumentales como la RMN, espectroscopia UV (usando el ensayo del ácido 2, 4, 6-trinitrobencenosulfónico o TNBS), espectrofotometría de fluorescencia (FS), infrarrojo cercano (NIR) e infrarrojo por transformada de Fourier (FT-IR) para confirmar la reticulación. Sin embargo, estas técnicas pueden tener limitaciones para identificar el entrecruzamiento en las cubiertas de las cápsulas cuando la desaceleración de la disolución se debe a pruebas de estrés o almacenamiento prolongado.
Estrategias para Mitigar el Entrecruzamiento
Superar el desafío del entrecruzamiento es crucial para el desarrollo de formulaciones de gelatina. Existen varias formas de mitigar este problema:
- Elección del tipo de gelatina: La gelatina tipo B demuestra una reticulación reducida en comparación con la gelatina tipo A.
- Inhibición de aldehídos (eliminadores de carbonilos): Compuestos como lisina, fenilalanina, glutamina, ácido p-aminobenzoico y glicina actúan como potentes eliminadores de compuestos carbonílicos, obstruyendo la interacción del aldehído con la gelatina y reduciendo significativamente la reticulación. La combinación de glicina con ácido cítrico es muy efectiva, ya que elimina los aldehídos y facilita la manipulación del pH.
- Otros inhibidores: La semicarbazida, la piperidina y el clorhidrato pueden modificar las propiedades de la cápsula, inhibiendo el entrecruzamiento.
- Uso de excipientes sin aldehídos: Optar por excipientes que no generen aldehídos es una vía prometedora.
- Condiciones de almacenamiento: Proteger las formulaciones contra la humedad, las fluctuaciones de temperatura y la exposición a la luz es fundamental para mantener la estabilidad y prevenir reacciones de reticulación.
- Pruebas de disolución de dos niveles: Un esfuerzo de colaboración entre la FDA de EE. UU., la Farmacopea de los Estados Unidos (USP) y el mundo académico llevó al desarrollo de estas pruebas, que incorporan enzimas en el medio de disolución para tener en cuenta la actividad enzimática in vivo. Esto es importante porque, aunque la reticulación ocurre principalmente in vitro, el comportamiento cambia notablemente in vivo debido a la presencia de enzimas en el entorno gastrointestinal que rompen los enlaces cruzados.
La siguiente tabla ilustra un método representativo de disolución de dos niveles:
| Fármaco | Tipo de Cápsula | Aparato | RPM | Medio de Disolución | Volumen | Tiempos de Muestreo Recomendados (minutos) | Actualizado |
|---|---|---|---|---|---|---|---|
| Lopinavir/ritonavir | Cápsula (gelatina blanda) | II (remo) | 50 | Nivel 1: Polioxietileno 0.5 M. 10 Lauril Éter con Fosfato de sodio monobásico 10 mM (pH 6.8); Nivel II: igual que arriba con No más de 1750 unidades USP/L de pancreatina | 900 | 10, 15, 30 y séptima | 06/18/2007 |
| Celecoxib | Cápsulas | II (remo) | 50, 100 y 200 mg: 50 rpm; 400 mg: 75 rpm | Nivel I Medio: Fosfato de sodio tribásico 0.04 M (pH 12) con 1% SLS. Medio inicial de nivel II: 750 ml de líquido gástrico simulado, USP (incluye pepsina); A los 20 minutos, mientras se agita, agregue 180 ml de concentraciones apropiadas de solución de SLS (para una concentración final de 1% de SLS). Añadir unos 70 ml de NaOH 1.2 N para ajustar el pH a 12. | Nivel I: 1,000 ml; Nivel II: 750 ml (inicial) 1,000 ml (finales) | 10, 20, 30, 45 y 60 | 07/01/2010 |
Gelatina vs. Cápsulas de HPMC: Una Comparación en el Contexto del Entrecruzamiento
La elección del material de la cápsula es estratégica y no meramente técnica, afectando el diseño de la formulación, las condiciones de almacenamiento, el estado legal y el alcance del consumidor. Aunque la gelatina ha sido el estándar tradicional, la hidroxipropilmetilcelulosa (HPMC) se ha convertido en una alternativa popular, especialmente para formulaciones sensibles.
La HPMC se crea mediante una modificación química de la celulosa vegetal, lo que la hace apta para veganos y vegetarianos. A diferencia de la gelatina, las cápsulas de HPMC tienen un bajo contenido de humedad (3-8%), son químicamente estables y físicamente resistentes en diferentes entornos. No favorecen el crecimiento microbiano ni reaccionan con muchos ingredientes activos sensibles porque no están basadas en proteínas. Esto significa que el HPMC es un polímero químicamente inerte, por lo tanto, nunca se reticula. Incluso en condiciones de almacenamiento húmedas o a altas temperaturas, las cápsulas de HPMC mantienen su perfil de disolución.
Sin embargo, la gelatina aún ofrece ventajas como una barrera superior al oxígeno, haciéndola ideal para ingredientes sensibles a la oxidación (ej., vitamina C, aceites de pescado en polvo), y su rentabilidad y maquinabilidad en máquinas de llenado de alta velocidad. El HPMC es más "transpirable", por lo que los ingredientes sensibles a la oxidación pueden requerir envases secundarios protectores.
La siguiente tabla presenta una comparación clave entre las cápsulas de gelatina y las de HPMC, destacando la relevancia del entrecruzamiento:
| Dimensión | Cápsulas de Gelatina | Cápsulas HPMC (Vegetarianas) | Conclusión Clave |
|---|---|---|---|
| 1. Origen de la materia prima | Colágeno animal (hueso/piel de bovino, piel de porcino). | Celulosa vegetal (derivado de la pulpa de pino o de la fibra de algodón). | HPMC (en línea con la tendencia mundial “Plant-Based”). |
| 2. Público objetivo | Mercado general de masas (no vegetarianos). | Vegetarianos, veganos, grupos religiosos (Halal/Kosher). | HPMC (aceptación universal; cero barreras culturales). |
| 3. Contenido de humedad | Alta (13% - 16%), depende del agua para ser flexible. | Bajo (3% - 8%), estructuralmente estable; no depende del agua. | HPMC (menor humedad = más seguro para los ingredientes sensibles). |
| 4. Aptitud higroscópica | ❌ Alto riesgo: los polvos higroscópicos arrastran agua de la cáscara, haciendo que la cápsula se vuelva frágil y quebradiza. | ✅ Excelente: su bajo contenido en humedad lo hace ideal para polvos y extractos de hierbas que necesiten humedad. | HPMC (flexibilidad de formulación mucho mayor). |
| 5. Riesgo de reticulación | ⚠️ El riesgo existe: puede reticularse con aldehídos o en condiciones de calor/humedad elevados, lo que provoca su insolubilidad (endurecimiento). | ✅ Sin riesgo: polímero químicamente inerte; la ausencia de reacción de reticulación garantiza una disolución uniforme. | HPMC (estabilidad física superior). |
| 6. Barrera de oxígeno | ✅ Excelente: bloquea eficazmente el oxígeno de forma natural; ideal para la vitamina C o los aceites de pescado. | ⚠️ Media: la permeabilidad es mayor que la de la gelatina; los ingredientes sensibles pueden necesitar un envasado secundario. | Gelatina (a menos que utilice Pullulan o HPMC especializado). |
| 7. Calefacción y almacenamiento | Sensible: se reblandece por encima de 60°C; es necesario un control estricto de la humedad (35-65% HR). | Robusto: soporta temperaturas más altas y menor humedad sin fracturarse. | HPMC (más seguro para el envío a climas cálidos/secos). |
| 8. Desintegración | Rápido: se disuelve rápidamente en el ácido gástrico (normalmente entre 5 y 10 minutos). | Consistente: arranque algo más lento pero predecible; menos afectado por las variaciones del pH. | Empate (ambos cumplen las normas de la farmacopea mundial). |
| 9. Resistencia mecánica | Fuerte, pero se vuelve quebradiza si se deshidrata. | Elástico y flexible; alta resistencia a la rotura durante el llenado. | HPMC (índice de defectos a menudo inferior en máquinas de alta velocidad). |
En India, un estudio encargado por el gobierno para analizar la viabilidad de usar cápsulas de HPMC como estándar para medicamentos concluyó que las cápsulas de gelatina son más eficaces, presentan mínimas complicaciones de fabricación y, en general, son la opción más segura para dosificar la medicación, a pesar de las presiones de grupos vegetarianos.
CÁPSULAS DE GELATINA DURA
La fabricación de cápsulas duras y blandas requiere cálculos precisos y su rendimiento puede variar, especialmente la velocidad de disolución. La gelatina tiene uno de los mejores índices de disolución, permitiendo una rápida absorción del API. Sin embargo, la exposición a condiciones inadecuadas de calor o humedad, o la presencia de ciertos aldehídos, puede provocar el entrecruzamiento. Debido a su baja humedad, la HPMC no está sujeta a estos problemas.
La gelatina, como proteína pura y de alta calidad derivada de subproductos de la industria cárnica, contribuye a la reducción de residuos y es un ingrediente de elección a nivel mundial. A diferencia de muchas alternativas, la gelatina no se considera un aditivo alimentario y, por tanto, no tiene un número E. La trazabilidad es vital en su producción, con estrictos controles de calidad y seguridad.