Este documento detalla los procedimientos para la identificación bioquímica y la confirmación serológica de microorganismos del grupo Enterobacterias, con un enfoque particular en la detección de Salmonella. Se describen métodos para el análisis de diversas muestras, incluyendo alimentos crudos, secos, en polvo y productos altamente contaminados.
Preparación de la Muestra y Enriquecimiento
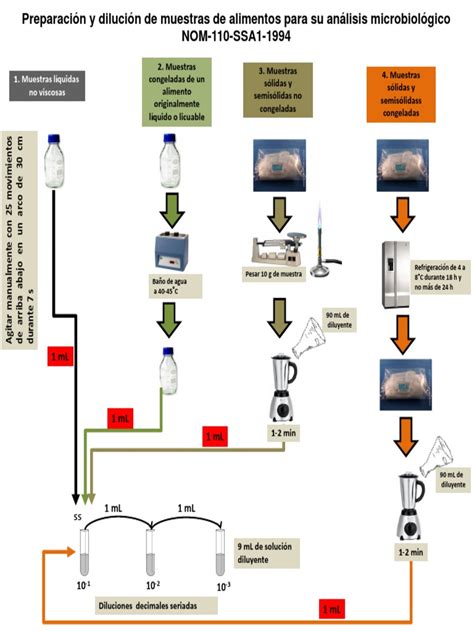
El proceso comienza con la preparación de la muestra analítica. Para muestras sólidas de 25 g o más, se utiliza un homogeneizador (stomacher) para mezclar la muestra con un caldo de cultivo en una proporción de 1:9 (muestra/caldo). Esta proporción puede ajustarse siempre que se mantenga la misma relación. Si la muestra es en polvo o molida, el paso de licuado puede omitirse. La mezcla debe realizarse durante un minuto a temperatura ambiente con la tapa bien enroscada.
Para productos crudos o altamente contaminados, se emplean porciones de 25 g de producto distribuidas en dos vasos para licuadora. Estas se inoculan directamente en matraces Erlenmeyer estériles de 500 ml. Cada muestra analítica se enriquecerá con caldo tetrationato. Alternativamente, se puede utilizar un matraz Erlenmeyer de 500 ml con 10 ml de caldo tetrationato y otro con 10 ml de caldo selenito cistina.
El pH de la mezcla se ajusta utilizando papel pH y, si es necesario, hidróxido de sodio 1N o ácido clorhídrico 1N estériles. Posteriormente, las muestras se incuban durante 24 ± 2 horas a 35ºC. Las muestras fuertemente contaminadas pueden incubarse a 42ºC por el mismo período.
Medios de Cultivo y Observación de Colonias
Se utilizan diversos medios de cultivo para el aislamiento y la identificación preliminar. El caldo rojo de fenol, que contiene sacarosa y rojo de fenol como indicador de pH, se emplea para evaluar la fermentación de carbohidratos. Si un microorganismo fermenta la sacarosa, el pH del medio disminuye, provocando un cambio de color de rojo a amarillo, y a menudo se observa formación de gas.
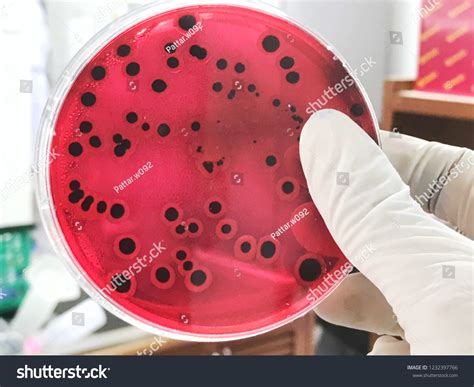
El medio de cultivo tetrationato y el caldo selenito cistina son importantes para el enriquecimiento selectivo. Tras la incubación, se observan las colonias en placas de agar. Las colonias de Salmonella suelen ser transparentes y pueden presentar un centro negro. Algunas colonias pueden mostrar un centro negro pronunciado, mientras que otras pueden aparecer completamente negras.
Pruebas Bioquímicas para la Identificación
Para la identificación bioquímica, se emplean varias pruebas clave:
Agar Triple Azúcar (TSI)
Se inoculan tubos de agar TSI mediante estría en la superficie inclinada y punción en el fondo. La fermentación de la lactosa y la sacarosa, así como la producción de sulfuro de hidrógeno (indicado por un color negro en el fondo del tubo), se evalúan tras la incubación.
Agar Lisina-Hierro (LIA)
Se inoculan tubos de LIA por estría en la superficie inclinada y punción en el fondo. La reacción en LIA es crucial para la identificación de Salmonella. Una reacción púrpura en todo el tubo indica descarboxilación de la lisina, un resultado típico para Salmonella. La ausencia de fermentación de la lactosa ni de la sacarosa también es característica.
Prueba de Ureasa
Se realizan pruebas de ureasa, tanto convencionales como rápidas, inoculando tubos de caldo urea. La producción de ureasa se detecta por un cambio de color en el medio. Los cultivos de Salmonella generalmente no producen ureasa.
Otras Pruebas Bioquímicas
A partir de los cultivos recuperados de TSI, se siembran pruebas bioquímicas adicionales para confirmar la identidad del microorganismo. Si los resultados son atípicos, se repiten las pruebas bioquímicas.
Confirmación Serológica (Prueba de Aglutinación)
La confirmación serológica se realiza mediante la prueba de aglutinación, utilizando sueros específicos para antígenos de Salmonella. Se prepara un cultivo formalizado del microorganismo a partir de una colonia aislada. Se mezclan gotas de este cultivo formalizado con suero anti-O y suero anti-H específicos en portaobjetos limpios.
Las mezclas se incuban en baño de agua a 48-50ºC durante aproximadamente un minuto. Se observa aglutinación en la mezcla de prueba, pero no en el control (cultivo formalizado sin suero o con suero no específico). Una aglutinación positiva confirma la presencia de Salmonella.
Es importante notar que:
- La mayoría de los cultivos de Salmonella (aproximadamente el 98%) dan resultados positivos en la prueba de aglutinación con sueros específicos.
- Algunas cepas de Salmonella pueden requerir la adición de 0,5 ml del cultivo formalizado a 0,5 ml de suero específico y incubación durante 24 ± 2 horas a 35ºC para la prueba al día siguiente.