Cada invierno, las zonas de alta montaña y los territorios que alcanzan temperaturas bajo cero se cubren de hielo y nieve, lo que genera situaciones potencialmente peligrosas para la circulación. La clave para gestionar estas condiciones reside en un fenómeno físico-químico: la capacidad de ciertas sustancias, como la sal, para reducir el punto de congelación del agua.
¿Qué es la depresión del punto de congelación?
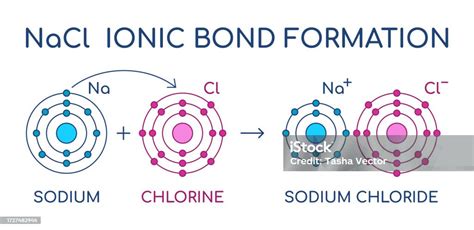
Por norma general, el agua pura se congela a 0 °C. Sin embargo, al añadir sal (cloruro de sodio, NaCl), la temperatura de congelación se reduce significativamente, pudiendo alcanzar los -21 °C. Este fenómeno se conoce como depresión del punto de congelación.
El agua se congela cuando sus moléculas se desaceleran lo suficiente como para formar una estructura cristalina regular. Cuando se agregan sales, los iones (cationes de sodio $Na^+$ y aniones de cloruro $Cl^-$) se interponen en el camino de las moléculas de agua. Estos iones atraen a las moléculas de agua e interfieren con la formación de la gran red sólida conocida como hielo. Como resultado, las moléculas de agua no pueden organizarse en un patrón sólido a la temperatura habitual.
Es importante destacar que este fenómeno es una propiedad coligativa de la materia. Esto significa que la depresión del punto de congelación depende del número de partículas presentes en la solución, no del tipo de partículas o de su masa. Por ejemplo, el cloruro de calcio ($CaCl_2$) es más efectivo que el cloruro de sodio ($NaCl$) porque, al disolverse, produce tres partículas (un ion de calcio y dos de cloruro) frente a las dos del cloruro de sodio.
Mezcla Frigorifica. Enfriar con Hielo y Sal. 🧊 + 🧂
Aplicaciones prácticas y seguridad vial
La sal es la sustancia más empleada habitualmente para prevenir la formación de hielo debido a su bajo coste y eficacia. Aunque el deshielo en carreteras se puede planificar con antelación, en ocasiones se requiere una respuesta inmediata. Actuar de forma preventiva es la estrategia más eficaz para evitar complicaciones en la circulación.
- Mantenimiento vial: Se extienden sales para disolverse en la delgada capa de agua sobre el hielo, bajando su punto de congelación y evitando que el hielo derretido se vuelva a congelar.
- Industria alimentaria: Se utilizan pequeñas cantidades de sales para prevenir la formación de grandes cristales de hielo durante la congelación, protegiendo así la textura y calidad de los alimentos.
- Sistemas industriales: En sistemas de enfriamiento, las sales bajan el punto de congelación del refrigerante, evitando que se solidifique en ambientes fríos.
Sin embargo, este proceso tiene sus contrapartidas. La mezcla de hielo y sal puede resultar perjudicial para el asfalto. Asimismo, en circunstancias extremas, se recurre a compuestos con un comportamiento higroscópico más agresivo, como el cloruro de magnesio, que actúa eficazmente a temperaturas aún más bajas.
Experimento: ¿Por qué el hielo se enfría al añadir sal?
Para observar este fenómeno, se puede realizar un experimento sencillo: si ponemos hielo en un recipiente a unos 3,4 °C y añadimos sal, la temperatura de la mezcla puede descender hasta los -11 °C. Esto ocurre porque la disolución de la sal provoca una reacción endotérmica, un proceso que absorbe energía (calor) del entorno, en este caso, del recipiente o de la bebida que se desee enfriar.
| Sustancia | Efecto sobre el punto de congelación |
|---|---|
| Agua pura | 0 °C (Referencia) |
| Agua con NaCl | Depresión significativa (hasta -21 °C) |
| Soluciones alcohólicas (ej. Vodka) | Inferior al agua pura |
Este principio incluso se aplica en tecnologías emergentes, como en el desarrollo de electrolitos para sistemas de almacenamiento de energía y baterías de alto rendimiento, donde se busca una operación estable en diversas condiciones ambientales.