La prueba de Tollens, nombrada en honor al químico alemán Bernhard Tollens, es una reacción química ampliamente reconocida en la química orgánica. Se utiliza principalmente para detectar la presencia de aldehídos y distinguir entre estos y las cetonas. Además, es un método para identificar otras sustancias con propiedades reductoras, como ciertos azúcares y alquinos con el triple enlace en la posición 1.
Esta prueba es conocida popularmente como la "prueba del espejo de plata" debido a la característica capa de plata metálica que se forma en las paredes del recipiente de laboratorio cuando el resultado es positivo.
Fundamento Teórico del Reactivo de Tollens
Aldehídos y Cetonas: Diferencias Estructurales y Reactividad
Los aldehídos son una clase de compuestos orgánicos cuya característica definitoria es la presencia de un grupo aldehído, o grupo -CHO, en la molécula. En un aldehído, el grupo carbonilo (C=O) se une a un átomo de hidrógeno y a un radical alquilo o arilo.
Las cetonas son compuestos químicos que contienen un grupo carbonilo (-CO-) unido a dos radicales que pueden ser iguales o diferentes. Aunque comparten similitudes estructurales y propiedades fisicoquímicas con los aldehídos, existen diferencias fundamentales que pueden demostrarse con pruebas como la de Tollens.
La principal diferencia radica en su capacidad de oxidación: los aldehídos se oxidan con facilidad a ácidos carboxílicos, mientras que las cetonas no lo hacen tan fácilmente. Esto se debe a la presencia de un átomo de hidrógeno unido al carbono del grupo carbonilo en los aldehídos, el cual está ausente en las cetonas. Este hidrógeno es sustraído durante la oxidación.
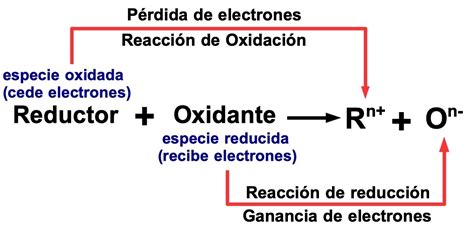
Mecanismo de Reacción Redox
La prueba de Tollens es un ejemplo clásico de reacción redox (oxidación-reducción). El reactivo de Tollens es una solución amoniacal que actúa como un agente oxidante suave.
El reactivo se obtiene disolviendo un precipitado negro de óxido de plata(I) en una solución acuosa de amoníaco. Durante este proceso, se forma un ion complejo diamina-plata(I), Ag(NH₃)₂⁺, que es soluble en agua y reacciona directamente con los aldehídos.
En presencia de un aldehído, ocurre la siguiente reacción:
- El grupo aldehído se oxida al grupo carboxilo (se forma un ácido carboxílico). El aldehído actúa como agente reductor.
- Simultáneamente, el ion plata del complejo diamina-plata(I) se reduce a plata metálica (Ag⁰). Los iones de plata actúan como agentes oxidantes.
Esta plata metálica se deposita en las paredes del recipiente, formando el característico "espejo de plata". Al mismo tiempo, se forman moléculas de amoníaco y agua. La aparición de este precipitado metálico es la evidencia de una prueba de Tollens positiva.
Toda la reacción se realiza en un ambiente ligeramente alcalino, y un aumento de la temperatura facilita la reacción.
Casos Especiales
Aunque la prueba de Tollens se asocia principalmente con aldehídos, algunos otros compuestos pueden dar un resultado positivo:
- El ácido fórmico (HCOOH), a pesar de ser un ácido carboxílico, contiene un grupo -CHO y exhibe propiedades reductoras, dando una prueba de Tollens positiva. Es el único ácido carboxílico que presenta esta propiedad.
- Algunos carbohidratos que no tienen un grupo aldehído pueden dar un resultado positivo debido a su isomerización en condiciones alcalinas.
- Las alfa-hidroxi cetonas (cetonas que contienen un grupo carbonilo unido a un carbono que soporta un grupo hidroxilo) también pueden dar pruebas positivas. Esta disposición de grupos se encuentra comúnmente en los azúcares.
Preparación del Reactivo de Tollens
El reactivo de Tollens es inestable y debe prepararse en el momento de su uso, nunca almacenándose por más de un par de horas, ya que puede formar nitruro de plata (Ag₃N), un compuesto altamente explosivo. La preparación debe realizarse con precaución y en un vaso de reacción limpio.

Pasos para la Preparación:
- En un recipiente limpio, añadir una sal de plata que se disocie fácilmente en iones en soluciones acuosas. Una opción común es una disolución acuosa de nitrato de plata (AgNO₃) al 5%. Por ejemplo, a 1 mL de disolución de AgNO₃ al 5%.
- Agregar hidróxido de sodio (NaOH) diluido, por ejemplo, 1 o 2 gotas de una disolución de NaOH al 5%. En este punto, se producirá la reacción de los cationes de plata con los aniones de hidróxido, resultando en la formación de un precipitado de hidróxido de plata (AgOH). Dado que el hidróxido de plata es muy inestable, se descompone casi inmediatamente, precipitando un óxido de plata(I) (Ag₂O) de color negro.
- Añadir amoniaco concentrado (NH₄OH) gota a gota, agitando suavemente, hasta que el precipitado de óxido de plata se disuelva completamente. Durante la disolución, se forma el ion complejo diamina-plata(I) soluble en agua, que es el componente activo del reactivo de Tollens.
El reactivo de Tollens es una solución transparente e incolora de pH básico.
Prueba de Tollens | Identificando Aldehídos | Oxidación de Aldehídos
Procedimiento Experimental para la Prueba de Tollens
Una vez preparado el reactivo de Tollens, se puede proceder con la prueba para identificar aldehídos o diferenciar entre estos y cetonas.
Realización de la Prueba
Para llevar a cabo la prueba de Tollens, se recomienda el siguiente procedimiento:
- En un tubo de ensayo limpio, agregar una cantidad específica del reactivo de Tollens (por ejemplo, 3 mL).
- Añadir la muestra a analizar (aldehído, cetona, etc.), por ejemplo, 2 mL. Es importante manipular las muestras volátiles cubriendo los recipientes adecuadamente.
- Calentar los tubos de ensayo en un baño maría tibio (sin agitar) durante aproximadamente 5 a 15 minutos. El uso de perlas de ebullición en el baño maría puede ayudar a una ebullición controlada.
Observaciones Típicas
Las observaciones de la prueba de Tollens varían según el compuesto analizado:
- Acetaldehído: Tras aproximadamente 12 minutos en baño maría, se observa la formación de un espejo de plata. Esto indica una prueba de Tollens positiva.
- Benzaldehído: Al mezclar con el reactivo de Tollens, puede percibirse una reacción exotérmica a temperatura ambiente. Con la aplicación de calor, la solución puede oscurecerse a un color plomo, y a los 5 minutos se manifiesta la presencia del espejo de plata. Esto también indica una prueba de Tollens positiva.
- Acetofenona: Después de aplicar calor durante 15 minutos, no se observa la aparición del espejo de plata. Esto implica una prueba de Tollens negativa, confirmando que la acetofenona es una cetona y no se oxida bajo estas condiciones.
- Butil metil cetona: Similar a la acetofenona, no se observa la aparición del espejo de plata tras 15 minutos de calentamiento. Esto indica una prueba de Tollens negativa.

Seguridad y Desecho
Es crucial manipular el reactivo de Tollens con precaución. Nunca se debe almacenar por periodos prolongados debido a la formación potencial de nitruro de plata, un compuesto altamente explosivo y sensible al impacto.
Después de realizar la prueba, la mezcla resultante debe ser acidificada con ácido diluido (como ácido nítrico diluido) antes de ser desechada. Esta acidificación descompone el complejo diamina-plata(I) y previene la formación de subproductos peligrosos.
tags: #reactivo #de #tollens #preparacion