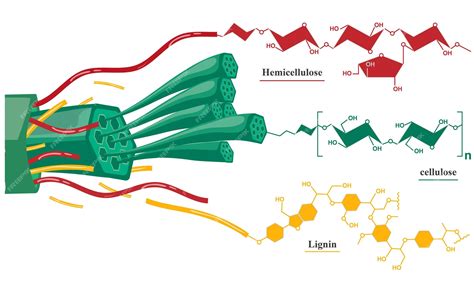
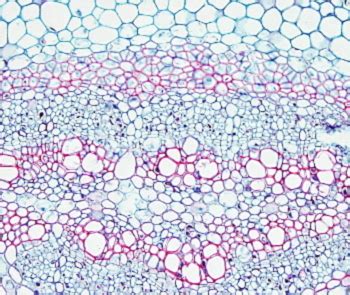
Así como para observar tejidos animales es imprescindible usar colorantes que diferencien el núcleo del citoplasma, en el caso de los tejidos y órganos vegetales se usan colorantes con afinidad por las paredes celulares. La tinción vegetal por excelencia se caracteriza por usar la safranina, que presenta afinidad por las paredes lignificadas (paredes secundarias), y un segundo colorante que puede ser el azul alcián o el verde luz (o verde rápido), ambos con afinidad por las paredes no lignificadas (paredes primarias).
Preparación y procesamiento de muestras
El procedimiento parte de muestras fijadas con FAA (formaldehído, alcohol, acético). Dependiendo de la técnica de corte, se pueden emplear diversos métodos:
- Cortes en vibratomo o microtomo de congelación: Permiten obtener cortes gruesos (mínimo de 40-50 μm) que se manipulan con pincel, realizando los pasos en pocillos pequeños con bajo volumen.
- Inclusión en parafina: Permite obtener cortes de gran calidad, generalmente por debajo de las 10 µm (rango habitual de 5 a 10 μm), procesándose de manera convencional.
Generalmente, el protocolo rápido para obtención de cortes histológicos vegetales supone el uso de vibratomo o micrótomo de congelación, aunque la parafina ofrece una resolución superior para detalles celulares finos.
Observación de células de epidermis de cebolla.
Protocolos de tinción
Existen diversas variantes según los colorantes utilizados para el contraste. La tinción con safranina es de carácter regresivo, lo que significa que la intensidad del color rojo se controla mediante los tiempos de diferenciación.
Protocolo con Safranina y Azul Alcián
- Etanol de 50°.
- Tinción en safranina.
- H2O destilada.
- Tinción en azul alcián (1 %, pH 2.5). Se recomienda poner en agitación al menos una hora y posteriormente filtrar.
- H2O destilada.
- Diferenciar con alcohol de 96° hasta que la mayor parte del tejido adquiera color azul claro.
- Etanol 100°.
- Xileno.
Protocolo con Safranina y Verde Rápido
- Etanol de 50°.
- Tinción en safranina (1 %, pH 2.5).
- H2O destilada.
- Etanol 96°.
- Tinción en verde rápido (1%) durante 60 segundos.
- Etanol 100°.
- Xileno.
Fundamentos fisicoquímicos de la coloración
Los colorantes son sustancias que tienen la capacidad de teñir células, estructuras o tejidos. En términos fisicoquímicos, el color se define a partir de las transiciones electrónicas al interior de los átomos, que permiten la absorción y emisión de radiación en el espectro visible (400 nm a 700 nm).
| Tipo de colorante | Característica | Ejemplo |
|---|---|---|
| Básicos | Carga positiva (catiónica), afinidad por ácidos nucleicos | Safranina, Azul de metileno |
| Ácidos | Carga negativa (aniónica), afinidad por estructuras citoplasmáticas | Eosina, Verde luz |
| Neutros | Combinación de ambos | Colorantes complejos |
La capacidad de un compuesto para actuar como colorante depende de los cromóforos (grupos funcionales con alta densidad electrónica) y los auxocromos (sustituyentes que alteran las longitudes de onda de absorción). En las asociaciones moleculares, la presencia de enlaces conjugados facilita la movilidad de los electrones, intensificando el color observado al microscopio.