La corrosión se define generalmente como la degradación de los metales a través de un proceso electroquímico natural. Este fenómeno es responsable de la formación de óxido en el hierro, el deslustre en la plata y la característica pátina azul-verdosa que se desarrolla en el cobre y sus aleaciones, como el bronce y el latón.
La corrosión es un problema industrial de gran magnitud, que puede ocasionar accidentes graves debido a la ruptura de piezas y representa un costo económico considerable. Se estima que cada pocos segundos se disuelven toneladas de acero en el mundo, sumando una cantidad importante al multiplicarse por la vasta cantidad de acero existente globalmente.
Principios Fundamentales de la Corrosión
La corrosión es, en esencia, la tendencia de los materiales a buscar su forma más estable o de menor energía interna. Cuando este proceso se origina por una reacción electroquímica de oxidación-reducción, su velocidad depende de factores como la temperatura, la salinidad del medio circundante y las propiedades intrínsecas de los metales.
Para que ocurra la corrosión electroquímica, se requiere la presencia de tres componentes fundamentales:
- Electrodos: un ánodo (donde ocurre la oxidación) y un cátodo (donde ocurre la reducción).
- Electrolito: un medio conductor, usualmente una solución acuosa, que permite el movimiento de iones.
- Conexión eléctrica: un camino para el flujo de electrones entre el ánodo y el cátodo, generalmente a través del propio metal.
Este conjunto de elementos forma una celda electroquímica o celda de corrosión. La diferencia de potencial entre el ánodo y el cátodo impulsa la migración de electrones. El metal o especie química con un potencial de reducción más negativo tiende a oxidarse (actuar como ánodo), mientras que aquel con un potencial de reducción más positivo tiende a reducirse (actuar como cátodo).
La transmisión de cargas eléctricas se realiza mediante electrones a través del metal (del ánodo al cátodo) y por iones en el electrolito.
Ejemplos Notables de Corrosión
La Estatua de la Libertad: Un Icono de la Corrosión
La icónica Estatua de la Libertad, reconocida por su altura, pose y distintivo color azul verdoso, es un ejemplo palpable de los efectos de la corrosión. Originalmente, la estatua, cuya "piel" está compuesta principalmente de cobre, era de color marrón. Con el tiempo, la exposición al aire provocó la oxidación del cobre.
Las reacciones de reducción-oxidación del cobre metálico en el ambiente son un proceso complejo. La quema de carbón, que a principios del siglo pasado a menudo contenía un alto contenido de azufre, generó compuestos que contribuyeron a la formación de la característica pátina azul-verde. Afortunadamente, esta pátina actúa como una capa protectora, impidiendo una mayor corrosión del cobre subyacente.

La Herrumbre del Hierro
Quizás el ejemplo más conocido de corrosión es la formación de óxido en el hierro. El hierro se oxida cuando se expone al oxígeno y al agua. Este proceso a menudo implica la creación de una celda galvánica en la superficie del hierro.
La corrosión puede ocurrir incluso en superficies de hierro o acero pintadas si la pintura se daña, por ejemplo, por un arañazo. En tales casos, la capa de pintura, si está intacta, impide el contacto del hierro con el agua y el oxígeno necesarios para la formación de óxido.
Tipos y Mecanismos de Corrosión
La corrosión puede manifestarse de diversas maneras, dependiendo de los materiales involucrados y las condiciones ambientales:
Corrosión Química (Corrosión Seca)
Ocurre en ambientes donde no hay conductividad iónica, típicamente en presencia de gases de escape, petróleo, ciertas sustancias orgánicas o gases como el hidrógeno, sulfuro de hidrógeno, monóxido de carbono o cloro. En la corrosión química, generalmente toda la superficie del material entra en contacto con el agente corrosivo, pero rara vez representa un riesgo significativo para la estructura.
Corrosión Electroquímica (Corrosión Húmeda)
Se desarrolla en ambientes capaces de conducir cargas eléctricas, como los electrolitos. El agua con gases o sales disueltas es un ejemplo común. En estas condiciones, se forman celdas galvánicas locales en la superficie del material, especialmente en puntos de contacto con la humedad. La presencia del electrolito cierra el circuito, permitiendo la corrosión electroquímica, que resulta en la oxidación de las superficies metálicas y la formación de depósitos, como el óxido.
Corrosión Generalizada o Uniforme
Afecta a toda la superficie del material de manera homogénea, deteriorándolo por completo. Aunque es el tipo de corrosión que provoca mayor pérdida de material, es relativamente fácil de predecir y controlar, por lo que los accidentes derivados de ella son poco comunes. Es frecuente en materiales de hierro no aleados con metales inoxidables.
Corrosión Localizada
Representa un mayor riesgo debido a su difícil detección, ya que se manifiesta en zonas específicas del material. Factores como la naturaleza del material, su geometría y las condiciones del medio influyen en su desarrollo.
Corrosión Galvánica
Se produce cuando dos metales de diferente naturaleza están en contacto físico o eléctrico en presencia de un electrolito. Forman una celda electroquímica donde el metal con menor potencial electroquímico se corroe. La relación entre las áreas de contacto de los metales es un factor crucial.

Corrosión por Picaduras (Pitting)
Se desarrolla en zonas estrechas donde la concentración de oxígeno es menor que en el resto del sistema. Estas zonas de baja concentración de oxígeno actúan como ánodos, propiciando el proceso de corrosión dentro de las fisuras.
Corrosión por Esfuerzo (Stress Corrosion Cracking - SCC)
Ocurre cuando un material está sometido a esfuerzos de tensión (internos o externos) y se forman pequeñas fisuras que inician el proceso de corrosión. Si los esfuerzos son cíclicos o fluctuantes, se habla de corrosión bajo fatiga.
Corrosión Microbiológica (MIC)
Algunos microorganismos son capaces de causar corrosión en superficies metálicas sumergidas. Ciertas especies utilizan el hidrógeno disuelto en el agua en sus procesos metabólicos, creando diferencias de potencial en el medio circundante. Su acción a menudo se asocia con el picado o la presencia de ácido sulfhídrico.
Otros Tipos de Corrosión
- Desaleación: En aleaciones metálicas, un elemento se separa selectivamente, dejando una estructura porosa con propiedades deficientes. Un ejemplo es la descincificación del latón, donde el zinc se separa de la matriz de cobre.
- Oxidación a Alta Temperatura: Ocurre en presencia de gases oxidantes como oxígeno, azufre o halógenos. Son reacciones puramente químicas, sin electrolito, por lo que también se conoce como corrosión seca.
- Ataque por Metal Líquido: Los metales líquidos atacan a los sólidos en sus puntos de mayor energía, como los límites de grano, generando grietas.
- Lixiviación Selectiva: Consiste en la separación selectiva de sólidos de una aleación. La corrosión grafítica del hierro fundido gris es un ejemplo, donde el hierro se disuelve dejando grafito.
- Disolución de Materiales Cerámicos: Los materiales cerámicos refractarios pueden ser disueltos por escorias en contacto con metales fundidos.
- Ataque Químico a Polímeros: Aunque materiales como el Teflón y el Vitón son muy resistentes, algunos solventes agresivos pueden separar las cadenas de los plásticos, provocando hinchazón y grietas.
Factores que Influyen en la Corrosión
La velocidad y el tipo de corrosión están influenciados por una variedad de factores:
- Composición del electrolito: El pH, la presencia de sales (ácidas o alcalinas) y la concentración de iones influyen significativamente. Las sales ácidas generalmente aceleran la corrosión, mientras que las alcalinas pueden actuar como inhibidores en algunos casos.
- Concentración de Oxígeno: En metales ferrosos, una mayor concentración de oxígeno tiende a acelerar la corrosión, ya que el producto corrosivo no protege eficazmente el material.
- Temperatura: La velocidad de corrosión generalmente aumenta con la temperatura, debido a la mayor difusión del oxígeno y la aceleración de las reacciones. Un aumento de 2°C puede duplicar la tasa de corrosión.
- Salinidad: La presencia de sales, especialmente en el agua de mar, actúa como un potente agente corrosivo.
- Humedad: El agua es un agente corrosivo fundamental y actúa como electrolito.
- Presencia de Ácidos y Bases: Estos compuestos son agentes corrosivos potentes, con los ácidos siendo generalmente más agresivos.
La Pasivación: Una Defensa Natural
Algunos metales, como el aluminio, el níquel y el cromo, tienen la capacidad de formar una capa de óxido sólida y estable sobre su superficie. Esta capa, llamada capa de pasivación, se adhiere fuertemente al metal y evita una mayor degradación. La pasivación es un fenómeno natural y una técnica anticorrosiva importante.
Prevención y Protección Contra la Corrosión
Dado el impacto económico y de seguridad de la corrosión, se han desarrollado diversas estrategias para su control y prevención:
1. Selección de Materiales y Diseño Adecuado
La primera línea de defensa es elegir materiales resistentes a la corrosión para el entorno específico de aplicación. Esto puede incluir el uso de aceros inoxidables, aleaciones de aluminio, cerámicas o polímeros. Un diseño que evite la acumulación de humedad o la creación de geometrías propicias para la corrosión localizada también es crucial.
2. Recubrimientos Protectores
Consiste en aplicar una capa de material resistente a la corrosión sobre la superficie del metal a proteger. Estos recubrimientos actúan como barreras físicas, impidiendo el contacto con el oxígeno y la humedad.
- Recubrimientos Orgánicos: Pinturas y otros polímeros resistentes a la degradación.
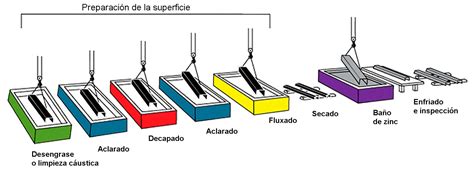
- Recubrimientos Metálicos: Incluyen métodos como el galvanizado (recubrimiento con zinc), la cromación o la estañación, aplicados por inmersión en caliente o electrólisis. El zinc, por ejemplo, ofrece protección incluso si la capa se daña, actuando como ánodo de sacrificio.
- Recubrimientos Cerámicos: Utilizados en aplicaciones de alta temperatura.
3. Inhibidores de Corrosión
Son sustancias químicas que, al añadirse al electrolito, reducen significativamente la velocidad de corrosión. Actúan de diversas maneras, como formando películas protectoras en la superficie metálica o alterando las reacciones anódicas o catódicas. Se utilizan en sistemas de enfriamiento, calderas y combustibles.
4. Protección Catódica
Este método convierte el metal a proteger en el cátodo de una celda galvánica. Esto se logra conectándolo a un metal más activo (más electronegativo), conocido como ánodo de sacrificio (como el zinc o el magnesio). El ánodo de sacrificio se corroe en lugar del metal protegido. Se utiliza comúnmente en estructuras enterradas o sumergidas, como tuberías y cascos de barcos.
⚡ ¿Qué es la protección catódica en electroquímica? Explicación concreta del término ⚡
5. Protección Anódica
A diferencia de la protección catódica, la protección anódica busca inducir un estado de pasivación en el metal mediante la inyección de una corriente externa controlada. Esto hace que el metal se vuelva más anódico, promoviendo la formación de una capa protectora estable.
6. Modificación del Entorno
Cambiar las condiciones ambientales puede mitigar la corrosión. Esto incluye controlar la composición química del entorno (reduciendo la acidez o la salinidad), así como modificar la temperatura y la humedad.
Diferencias Clave: Oxidación vs. Corrosión
Aunque a menudo se usan indistintamente, existen diferencias importantes:
- Oxidación: Es un proceso superficial que ocurre cuando un metal reacciona con el oxígeno, formando una capa de óxido. Esta capa puede ser eliminada con limpieza.
- Corrosión: Es un proceso químico y/o electroquímico más complejo que implica la interacción del metal con su entorno (oxígeno, humedad, químicos). Penetra más allá de la superficie, pudiendo causar un deterioro significativo, pérdida de resistencia y debilitamiento estructural. La corrosión es, en general, un proceso irreversible.
El deterioro causado por la corrosión tiene un impacto económico considerable, afectando la durabilidad, seguridad y funcionalidad de estructuras, vehículos y maquinaria. La prevención y el mantenimiento adecuado son esenciales para mitigar estos efectos.