¿Qué es la Estructura Terciaria de una Proteína?
La estructura terciaria de una proteína es la distribución tridimensional de todos los átomos que la constituyen, refiriéndose a la forma tridimensional única de la proteína como un todo. Se forma sobre la disposición de la estructura secundaria de un polipéptido al plegarse sobre sí misma, originando una conformación globular. A diferencia de la disposición lineal de la estructura primaria o de los patrones regulares de las estructuras secundarias, la estructura terciaria de una proteína se refiere a la forma tridimensional que alcanza una única molécula de proteína. Esta estructura es el resultado del plegamiento y la flexión de la cadena principal de la proteína.
Generalmente, en la estructura terciaria los aminoácidos apolares se sitúan hacia el interior de la proteína y los polares hacia el exterior, de manera que puedan interactuar con el agua circundante. La estructura terciaria está íntimamente ligada al correcto funcionamiento bioquímico de la proteína y, en este estado, la proteína ya puede cumplir sus complejas funciones biológicas.
La distinción entre las estructuras primaria, secundaria y terciaria de las proteínas está relacionada con los grados de complejidad y organización de estas biomoléculas. Estas variaciones son cruciales para comprender su función en el contexto fisiológico:
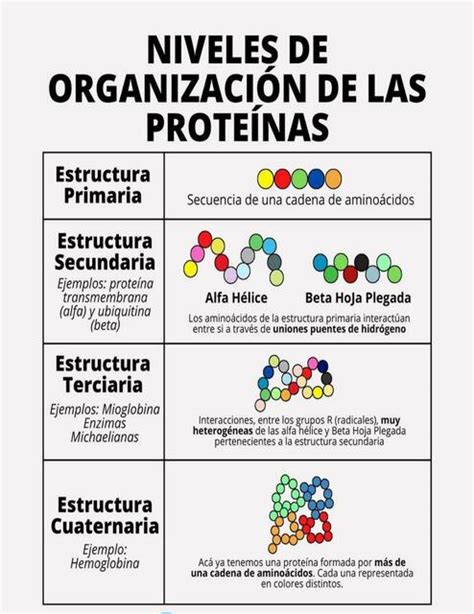
- Estructura primaria: Es la secuencia de aminoácidos que forman la cadena polipeptídica.
- Estructura secundaria: Consiste en el plegamiento local de la cadena polipeptídica en estructuras como hélices alfa y láminas plegadas beta.
- Estructura terciaria: Se refiere a la estructura tridimensional completa de una proteína, resultante del plegamiento posterior de las estructuras secundarias.
Tipos de Estructuras Terciarias
Las dos posibles estructuras terciarias que pueden originarse son:
- Estructura globular: Tiene forma de "ovillo", es soluble y es típica de las hormonas o los enzimas.
- Estructura fibrilar (o fibrosa): Se caracteriza por dar a la proteína forma de filamento y ser insoluble. Ejemplos de proteínas con esta estructura son la alfa o la beta-queratina y el colágeno.
Fuerzas e Interacciones que Estabilizan la Estructura Terciaria
La conformación globular se mantiene estable debido a la existencia de enlaces entre los radicales R de los aminoácidos. Una intrincada red de enlaces garantiza que la estructura tridimensional de la proteína permanezca intacta, permitiéndole interactuar adecuadamente con su entorno y desempeñar las funciones que le han sido asignadas. Cuatro tipos principales de interacciones atractivas determinan la forma y estabilidad de la estructura terciaria de las proteínas, además de las fuerzas de Van der Waals.
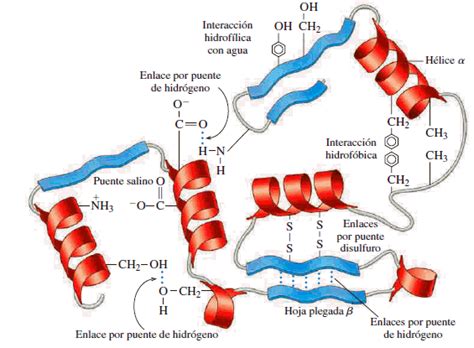
La estructura de las proteínas está estabilizada por diferentes tipos de enlaces:
- Enlaces peptídicos: Son enlaces covalentes que se forman entre el grupo carboxilo de un aminoácido y el grupo amino de otro aminoácido, constituyendo el esqueleto principal de la proteína.
- Puentes disulfuro: Estos enlaces covalentes se producen entre los átomos de azufre de dos residuos de cisteína que se encuentran próximos entre sí, formándose una cistina mediante oxidación.
-CH2-S-S-CH2- - Uniones iónicas (o puentes salinos): Son el resultado de atracciones electrostáticas entre cadenas laterales de aminoácidos con carga positiva y negativa. Los grupos cargados normalmente se encuentran en la superficie de la proteína y determinan el correcto plegamiento al poder interaccionar con el agua de solvatación.
- Enlaces de hidrógeno: Se forman entre un átomo de oxígeno o nitrógeno altamente electronegativo y un átomo de hidrógeno unido a otro átomo de oxígeno o nitrógeno, como los que se encuentran en las cadenas laterales de aminoácidos polares. En la estructura terciaria, proporcionan una estabilización adicional, sobre todo en las partes de la proteína donde se unen las estructuras secundarias.
- Interacciones hidrofóbicas: Se dan entre las cadenas laterales de los aminoácidos hidrofóbicos. Estos aminoácidos suelen disponerse en el interior de la proteína, evitando las interacciones con el agua, formando el corazón hidrofóbico. Este tipo de fuerzas interviene en el correcto plegamiento de la proteína.
- Fuerzas de Van der Waals: Son atracciones eléctricas débiles y transitorias entre diferentes átomos, resultantes de fluctuaciones en las nubes electrónicas que crean dipolos temporales. Aunque débiles, su gran número puede contribuir significativamente a la estabilidad estructural de las proteínas.
La Importancia de la Estructura Terciaria para la Función Proteica
Se puede afirmar que de la estructura terciaria derivan las propiedades biológicas de las proteínas, puesto que la disposición en el espacio de los diferentes grupos funcionales de la proteína condiciona su capacidad de interacción con otros grupos y ligandos. La estructura terciaria desempeña un papel crucial en la determinación de la funcionalidad de la proteína, ya que la forma tridimensional sutilmente orquestada por el proceso de plegamiento es fundamental para su interacción con otras moléculas y el desempeño de sus funciones dentro de la célula.
La capacidad de una proteína para unirse a otras moléculas, a menudo conocidas como sus ligandos, viene determinada por la forma específica y las características químicas del bolsillo de unión, que se forma como parte de la estructura terciaria. Una amplia gama de funciones surge de la forma única de la proteína y de las propiedades químicas resultantes.
Ejemplos de Funcionalidad y Estructura Terciaria
Para ilustrar la relevancia de la estructura terciaria para la función de las proteínas, consideremos algunos ejemplos característicos:
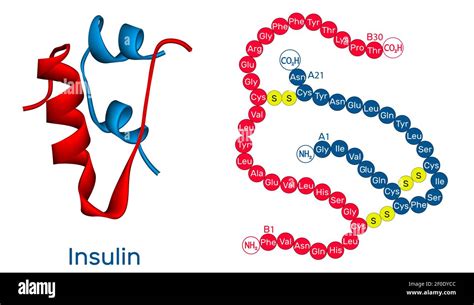
- Insulina: Comienza como una cadena de aminoácidos (estructura primaria), luego se enrolla en una hélice alfa (estructura secundaria), y finalmente, estas hélices se pliegan sobre sí mismas en una forma tridimensional (estructura terciaria). Esta forma es atraída por las moléculas de glucosa y puede unirse a ellas, controlando eficazmente la cantidad de azúcar en el torrente sanguíneo.
- Hemoglobina: Esta metaloproteína, que se encuentra en los glóbulos rojos, transporta oxígeno de los pulmones al resto del cuerpo. Su estructura consta de cuatro cadenas polipeptídicas, cada una con un grupo hemo individual. La combinación de estas cadenas y su disposición en la estructura terciaria permiten a la hemoglobina realizar su función única.
- Mioglobina: Cuya función es almacenar oxígeno en las células musculares, está formada por una sola cadena polipeptídica con un solo grupo hemo. Tanto la hemoglobina como la mioglobina ilustran perfectamente cómo las variaciones en la estructura terciaria pueden dar lugar a diferentes capacidades y funciones de las proteínas en el organismo.
- Albúmina: Es la proteína más abundante en el plasma sanguíneo humano. La albúmina sérica humana (HSA) es una biomolécula monomérica multidominio con un total de 585 aminoácidos. Tiene forma de corazón, donde los tres dominios, I, II y III, contienen cada uno dos subdominios A y B, que son estructuralmente similares. Aunque las albúminas no tienen una estructura cuaternaria, su estructura terciaria es compleja y versátil, lo que les permite unirse a una amplia gama de sustancias endógenas y exógenas.
Predicción y Determinación de la Estructura Terciaria
La predicción de la estructura tridimensional (3D) de las proteínas a partir de su secuencia de aminoácidos ha sido un desafío de investigación que ha perdurado por más de cinco décadas. Sin embargo, recientemente, se ha logrado un avance en este campo mediante el desarrollo de un método computacional que demuestra su capacidad para predecir de manera regular las estructuras de proteínas a nivel atómico, incluso en casos donde no se dispone de una estructura similar previamente conocida.
AlphaFold y la Inteligencia Artificial
Este avance se basa en un modelo impulsado por redes neuronales y tecnología de inteligencia artificial. AlphaFold, desarrollado por DeepMind, es un sistema de inteligencia artificial que se vale de redes neuronales profundas para predecir la estructura tridimensional de las proteínas. Su funcionamiento radica en tomar la secuencia de aminoácidos de una proteína como entrada y analizar las interacciones entre estos aminoácidos.
Descubriendo AlphaFold 3: La Revolución en la Predicción de Estructuras Proteicas"
Técnicas Experimentales
Tan importante como comprender qué es la estructura terciaria de una proteína son las técnicas que utilizan los científicos para identificarla y examinarla. Estas prácticas son fundamentales para el ámbito más amplio de la ingeniería de proteínas y la comprensión de la función de una molécula en su contexto biológico. La estructura terciaria detallada de una proteína puede determinarse mediante algunos procedimientos diferentes, que requieren instrumentación compleja y riguroso análisis computacional:
- Cristalografía de Rayos X: Es una de las herramientas más potentes para determinar la estructura de una proteína hasta el nivel atómico. El primer paso consiste en precipitar la proteína en un cristal sólido, que se bombardea con radiación de rayos X. Cuando los rayos X atraviesan y rebotan en los átomos del cristal, producen un patrón de difracción. Las primeras estructuras proteicas que se resolvieron fueron las de la mioglobina y la hemoglobina a finales de la década de 1950 y principios de la de 1960, trabajo que valió el Premio Nobel de Química a John Kendrew y Max Perutz.
- Espectroscopia de Resonancia Magnética Nuclear (RMN): Es otro método empleado en biología estructural para descifrar la estructura terciaria de las proteínas. Es una alternativa importante a la cristalografía de rayos X, sobre todo para las proteínas que no cristalizan fácilmente, ya que permite que las proteínas permanezcan en solución, asemejándose más a las condiciones fisiológicas. Sin embargo, la RMN no puede utilizarse para proteínas muy grandes debido a la complejidad que aumenta con el tamaño de la proteína, y la calidad de la información depende de la pureza y solubilidad de la muestra. Kurt Wüthrich recibió el Premio Nobel de Química en 2002 por su trabajo en RMN.
Transportadores de Glucosa (GLUTs y SGLTs): Estructura General y Función
Las hexosas como la glucosa, galactosa y fructosa sirven como moléculas de combustible básicas para las células eucariotas. Sin embargo, estas moléculas son incapaces de difundir directamente a través de las membranas celulares, por lo que requieren proteínas transportadoras especializadas para entrar y salir de las células. La membrana celular, de naturaleza lipídica, es relativamente impermeable a moléculas polares como la glucosa, por lo que la naturaleza desarrolló moléculas proteicas que cruzan completamente la membrana y son capaces de formar "poros" que comunican el exterior con el interior celular, permitiendo el flujo de moléculas.
Los transportadores de glucosa presentes en las células de los organismos superiores se clasifican en dos grandes familias:
- La Familia de los GLUTs (Glucose Transporters).
- La Familia de los co-transportadores de sodio y glucosa (SGLTs, Sodium/Glucose Transporters).
Los transportadores de membrana que median la transferencia de solutos comparten varias características:
- Especificidad: Cada transportador es específico para una sola sustancia o un grupo muy emparentado de estas.
- Saturación: La capacidad de transporte puede alcanzar un máximo cuando todos los sitios de unión para el soluto a transportar están ocupados.
- Competición: Ocurre cuando más de una sustancia es capaz de ser transportada por el sistema transportador; el soluto a mayor concentración será preferentemente transportado.
Familia de los GLUTs
La familia de los GLUTs es muy extensa, con más de 140 miembros distribuidos entre diferentes especies. Según la información obtenida de la secuencia de aminoácidos por medio de librerías de ADNc, todos poseen una estructura básica similar: 12 dominios transmembrana. Igualmente, todos parecen estar glicosilados en alguna de sus asas extracelulares. Hasta hace diez años solo se conocían 6 transportadores, pero esta familia ha crecido rápidamente hasta llegar a 14 miembros (GLUTs 1-14). El impacto de estos descubrimientos se nota en los procesos en que se involucran estas proteínas, como el control de la glicemia, la absorción de glucosa y fructosa en el intestino delgado, la reabsorción de glucosa a nivel tubular renal y yeyuno, y la incorporación de glucosa al músculo durante el ejercicio.
La fructosa se absorbe mediante otro tipo de transportador, el GLUT-5, una proteína que atraviesa la membrana 12 veces. Finalmente, el paso de la glucosa y la fructosa hacia la sangre se lleva a cabo a través del GLUT-2, un transportador de baja afinidad y alta capacidad de transporte.
Familia de los SGLTs
En el epitelio intestinal y en el epitelio de los túbulos contorneados proximal y distal existen sistemas de co-transporte de glucosa acoplados a Na+ que permiten la absorción rápida de esta molécula desde el íleo hacia el sistema portal, y la reabsorción de la glucosa filtrada en el glomérulo nuevamente al torrente circulatorio. Este sistema se denomina SGLT, del cual se conocen 6 isoformas (SGLT1-6) que aprovechan el transporte del Na+ a favor de su gradiente de concentración para generar una corriente electroquímica que produce los cambios conformacionales necesarios para la traslocación de la glucosa a través de la membrana plasmática. Al comparar las estructuras primarias, SGLT-2, SGLT-3 y SGLT-4 tienen un 70%, 59% y 54% de homología con SGLT-1, respectivamente.
SGLT-1 (SLC5A1)
El gen del SGLT-1 se denomina SLC5-A1 y fue aislado a partir de librerías de cDNA de intestino delgado de conejo. Su transcripto es una proteína de 664 aminoácidos y 73 KDa con una estructura secundaria formada por 14 α-hélices cuyos extremos amino y carboxilo terminales se encuentran en el espacio extracelular. El SGLT-1 es el principal transportador de monosacáridos (glucosa, galactosa y manosa) en el intestino delgado, co-transportando 2 iones Na+ y una molécula de glucosa a razón de unas 1.000 moléculas por segundo. Se organiza en forma de 14 alfa-hélices que cruzan la membrana plasmática la misma cantidad de veces. En el ser humano, este transportador se expresa primariamente a nivel del íleon, el sitio fundamental de absorción de monosacáridos.
El proceso de absorción de la glucosa, galactosa y fructosa en el borde en cepillo intestinal ocurre en 4 fases:
- Unión de dos iones Na+ a la cara externa del transportador, lo que produce un cambio conformacional que permite el acoplamiento de 1 molécula de glucosa o galactosa.
- Transferencia del Na+ y del monosacárido hacia la cara citoplasmática del transportador gracias a un segundo cambio conformacional ocasionado por la glucosa, que involucra la rotación y el re-arreglo de la estructura α-helicoidal del SGLT-1.
- Una vez en la cara interna del transportador, la glucosa se disocia del mismo y pasa al citosol para luego expulsar los 2 iones Na+, restituyendo al transportador a su forma libre de ligando.
- Finalmente, ocurre un cambio de conformación que permite la fijación de otra molécula de glucosa y 2 Na+ en el lado extracelular.
Este proceso es eficiente gracias a la baja afinidad del sitio de unión intracelular por la glucosa y el sodio, junto con la baja concentración intracelular de Na+ en comparación con la extracelular y luminal. El gradiente electroquímico de Na+ entre la luz intestinal y la célula epitelial se mantiene gracias a la bomba de Na+/K+ situada en la membrana basolateral, lo que impulsa la absorción eficiente de la glucosa.
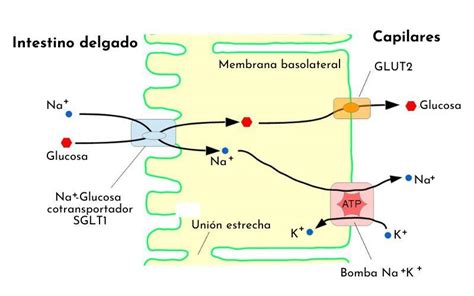
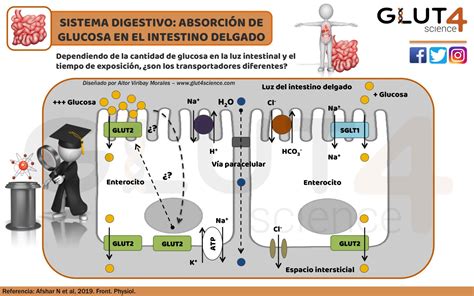
Co-transporte de Agua por SGLT-1
Un aspecto importante de la absorción de Na+ y glucosa es el co-transporte de agua desde la luz intestinal al interior de la célula epitelial y de allí hacia el compartimento intravascular. Investigaciones recientes han determinado que el SGLT-1 se comporta como un transportador de agua, movilizando unas 260 moléculas de agua por cada ciclo de transporte de 2 iones Na+ y cada molécula de glucosa, lo cual representa unos 5 litros de agua al día.
Desnaturalización y su Impacto en la Estructura Terciaria
La estructura terciaria de una proteína es sensible a cambios en su entorno. Si se sustituye un aminoácido por otro (alterando la estructura primaria), se alterará la estructura tridimensional de la proteína, ya que no se formará alguno de los enlaces que la estabilizan. La desnaturalización es el proceso en el que la proteína pierde su estructura tridimensional nativa, lo que generalmente implica la pérdida de su función biológica. Este cambio puede ser causado por factores como variaciones de temperatura, pH, concentración salina o la presencia de agentes químicos.
tags: #estructura #terciaria #glut #6