La tecnología CRISPR-Cas9 se ha consolidado como una herramienta revolucionaria en la edición genética, permitiendo la modificación precisa del ADN de las plantas para lograr cambios específicos en sus características. A diferencia de la transgénesis tradicional, CRISPR posibilita la introducción de pequeñas alteraciones en genes propios de la planta, sin necesidad de incorporar ADN de otras especies. Este enfoque abre la puerta a mejoras genéticas más rápidas y altamente específicas.
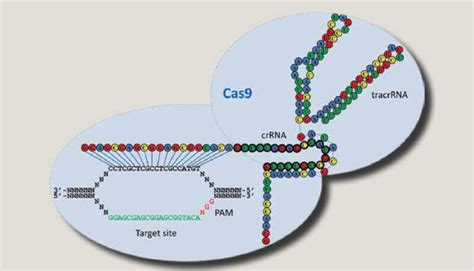
El sistema CRISPR-Cas9 se inspira en un mecanismo natural de defensa presente en las bacterias. Su funcionamiento se basa en dos componentes principales:
- ARN guía (gRNA): Una molécula diseñada para reconocer una secuencia específica del ADN vegetal.
- Proteína Cas9: Una enzima que actúa como unas "tijeras moleculares" para cortar el ADN.
En la práctica, CRISPR permite obtener plantas con modificaciones análogas a las que podrían surgir de forma natural o mediante mutagénesis, pero de una manera considerablemente más rápida y controlada. El proceso se desarrolla de la siguiente manera:
- El ARN guía localiza el gen objetivo. El gRNA se diseña para ser complementario a una secuencia específica dentro del genoma de la planta.
- La proteína Cas9 verifica el punto de corte mediante la señal PAM. Para que Cas9 realice el corte, el ADN objetivo debe contener cerca una pequeña secuencia conocida como PAM (Protospacer Adjacent Motif). Esta señal actúa como un mecanismo de seguridad: sin la presencia de PAM, Cas9 no cortará, incluso si el gRNA reconoce la secuencia deseada.
- Cas9 corta el ADN en el punto exacto. Una vez que el gRNA se une al ADN y Cas9 reconoce la señal PAM, la proteína efectúa un corte en ambas hebras del ADN.
A partir de este punto, el resultado final no depende de Cas9, sino de cómo la propia planta repara la ruptura del ADN. Las células vegetales, al igual que cualquier célula viva, no pueden permanecer con el ADN dañado y activan mecanismos de reparación:
- Reparación por NHEJ (unión de extremos no homólogos): Este es el mecanismo más frecuente en plantas. La célula vuelve a unir los extremos rotos del ADN de forma rápida, aunque a menudo imperfecta.
- Reparación por HDR (recombinación dirigida): Esta vía es menos común en plantas, pero permite introducir cambios más precisos en el ADN.
En resumen, el sistema CRISPR no "reescribe" directamente el ADN; en su lugar, induce un corte en un sitio específico, y es el proceso de reparación natural de la planta el que genera la modificación genética deseada.
Desafíos y Métodos de Edición Genética en Plantas
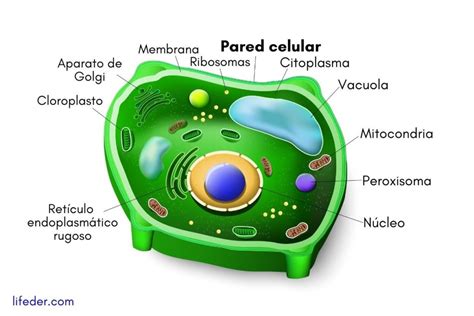
Aunque el mecanismo CRISPR-Cas9 es universal, la edición genética en plantas presenta particularidades que la diferencian de la edición en bacterias o animales. Uno de los principales obstáculos es la pared celular, una estructura rígida que rodea a las células vegetales y dificulta la entrada de moléculas grandes como Cas9 y el ARN guía.
Otro desafío significativo es la necesidad de regenerar una planta completa a partir de células editadas. En la mayoría de las especies, la edición ocurre en un número limitado de células. Para obtener una línea genética estable, estas células deben ser capaces de regenerar una planta entera a través de técnicas de cultivo in vitro, como la formación de callos, la embriogénesis somática o el desarrollo de brotes.
Además, en cultivos poliploides (con múltiples juegos de cromosomas), la existencia de varias copias de un gen puede complicar el proceso. Si no todas las células se editan de manera uniforme, la planta regenerada puede presentar un mosaico de células editadas y no editadas, fenómeno conocido como quimerismo.
Para que el sistema CRISPR funcione en plantas, es fundamental que la proteína Cas9 y el ARN guía logren acceder al núcleo de una célula vegetal. Los métodos más comunes para introducir estos componentes son:
- Transformación con Agrobacterium tumefaciens: Este es el método más empleado para muchas especies dicotiledóneas. La bacteria Agrobacterium tumefaciens se utiliza como vector natural para transferir el material genético deseado a las células vegetales.
- Biobalística (pistola de genes): Esta técnica consiste en "disparar" microproyectiles recubiertos con ADN o con complejos Cas9-gRNA directamente a tejidos vegetales.
- Protoplastos: En algunos casos, se eliminan las paredes celulares para obtener protoplastos (células vegetales sin pared), que son más receptivos a la transformación.
En la práctica, estas vías de entrega a menudo se combinan con técnicas de cultivo in vitro y rigurosos procesos de selección de las líneas editadas.
Flujo de Trabajo para la Aplicación de CRISPR en Mejoramiento Vegetal
La aplicación de CRISPR-Cas9 en plantas va más allá de la simple edición genética; implica un flujo de trabajo completo que abarca desde la concepción de la idea hasta la validación de nuevas líneas genéticas. Los pasos clave incluyen:
1. Definición del Rasgo y el Gen Objetivo
El proceso comienza con una hipótesis clara: identificar el rasgo agronómico que se desea mejorar (resistencia a enfermedades, tolerancia al estrés ambiental, calidad del producto, etc.) y determinar qué genes están implicados en dicho rasgo.
2. Diseño de Guías (gRNA)
Se diseñan una o varias secuencias de ARN guía que reconozcan de manera específica el gen objetivo. Es crucial evitar regiones genómicas similares que puedan llevar a cortes no deseados (efectos fuera de objetivo).
3. Elección del Formato de Edición y Construcción del Sistema CRISPR
Se determina si se busca inactivar un gen (knock-out) o introducir modificaciones específicas, y se construyen los vectores o complejos necesarios para expresar Cas9 y el gRNA.
4. Introducción de CRISPR en el Material Vegetal (Delivery)
Se selecciona el método de entrega más adecuado según la especie y el tejido vegetal a editar. Las opciones comunes incluyen Agrobacterium tumefaciens, biobalística o la transformación de protoplastos.
5. Regeneración de Plantas Completas a partir de Células Editadas
Las células transformadas se cultivan en medios de cultivo in vitro, estimulando la formación de callos, brotes y raíces hasta obtener plantas regeneradas.
6. Selección y Detección de las Líneas Editadas
Se emplean marcadores moleculares y técnicas de cribado para identificar las plantas que han sido editadas con éxito en el gen objetivo.
7. Validación del Fenotipo
No es suficiente con editar el gen; es fundamental comprobar el efecto real del cambio genético en el organismo. Esto implica evaluar si el rasgo deseado se ha manifestado.
8. Generación de Líneas Estables y Evaluación en Condiciones Reales
Finalmente, se desarrollan líneas genéticas estables y se evalúan su rendimiento y características en condiciones de campo o de producción.
Ejemplo Práctico: Mejora de la Firmeza en Frutillas
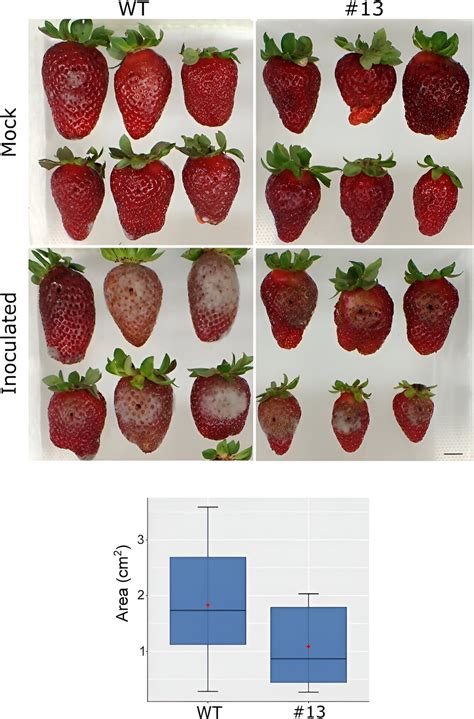
Un ejemplo ilustrativo de la aplicación de CRISPR en cultivos es el estudio realizado por investigadores de la Universidad de Málaga sobre la frutilla (Fragaria × ananassa). El objetivo era mejorar la firmeza del fruto, reducir el ablandamiento poscosecha y potenciar la resistencia a hongos patógenos como Botrytis cinerea.
La frutilla, a pesar de su valor nutricional y sabor, sufre un rápido ablandamiento debido al desmontaje de las paredes celulares durante la maduración, lo que limita su vida útil y genera pérdidas económicas. Las enzimas pectinasas, y en particular las poligalacturonasas (PG), juegan un papel crucial en este proceso de ablandamiento.
Los investigadores aplicaron la edición genética con CRISPR/Cas9 sobre el gen FaPG1, identificado como clave en el ablandamiento del fruto. Mediante la inactivación de este gen, lograron:
- Aumentar significativamente la firmeza del fruto en las líneas editadas.
- Observar una reducción en las tasas de ablandamiento poscosecha.
- Demostrar una mayor resistencia a la pudrición fúngica, incluyendo Botrytis cinerea.
Este estudio, publicado en Horticulture Research, subraya el potencial de la edición genética para mejorar las cualidades poscosecha de frutas y hortalizas, contribuyendo a la reducción del desperdicio alimentario y a minimizar su impacto socioambiental.
Otros Ejemplos y Potencial de CRISPR en Agricultura
La capacidad de CRISPR para realizar modificaciones precisas y eficientes ha impulsado su aplicación en una amplia gama de cultivos, abordando diversos desafíos agronómicos:
- Tomates y Kiwis Tolerantes a la Salinidad y Sequía: Investigadores chilenos están utilizando CRISPR/Cas9 para desarrollar nuevas variedades de tomates y kiwis más resistentes a condiciones de estrés abiótico, como la salinidad y la escasez de agua. Se estudian variedades nativas con alta resistencia natural, como el tomate "Poncho Negro", y se busca mejorar genéticamente otras de gran valor comercial.
- Maíz con Mayor Rendimiento: En China y Alemania, se ha silenciado un gen limitante en la producción de granos de maíz mediante CRISPR, lo que ha resultado en un aumento del 10% en el número de hileras de granos por mazorca y, consecuentemente, en el rendimiento de la cosecha.
- Verduras de Mostaza con Sabor Suave: La empresa Pairwise ha utilizado CRISPR para eliminar uno de los dos componentes responsables del amargor en las verduras de mostaza, creando variedades con un sabor más agradable para los consumidores.
- Ganado Bovino con Pelaje "Resbaladizo": La empresa Reombinetics empleó CRISPR para conferir al ganado vacuno una variante genética que produce un pelaje "resbaladizo", una característica natural que ayuda a los animales a tolerar mejor el calor en zonas subtropicales y tropicales.
- Papas Resistentes a Enfermedades: Se están llevando a cabo ensayos de campo con papas editadas genéticamente para evaluar su comportamiento y resistencia a enfermedades, como la marchitez bacteriana del plátano (BXW), que afecta a todas las especies de plátanos cultivados.
La edición del genoma mediante CRISPR-Cas se ha convertido en una herramienta poderosa para generar variabilidad genética de manera precisa y específica, abriendo una nueva era en el cultivo de plantas. Su aplicación abarca desde la mejora de la resistencia a enfermedades y plagas, la tolerancia a condiciones ambientales adversas, hasta el incremento del valor nutricional y funcional de los alimentos, la optimización del rendimiento y la reducción de compuestos indeseados.
CRISPR y la Edición Genética
El crecimiento exponencial en las publicaciones científicas sobre edición genómica basada en CRISPR desde 2013 evidencia su creciente importancia. Si bien los cultivos hortícolas son uno de los principales focos de aplicación, la técnica se está extendiendo a una amplia variedad de especies. La ausencia de transgenes en muchos de los cultivos desarrollados con CRISPR es un rasgo importante a considerar en los marcos regulatorios para su comercialización.
La velocidad de adopción de esta tecnología en el ámbito científico y comercial dependerá en gran medida de los aspectos regulatorios relacionados con la bioseguridad. Sin embargo, los primeros alimentos mejorados con CRISPR ya están llegando a los consumidores, demostrando el potencial de esta herramienta para afrontar desafíos globales como la seguridad alimentaria, la sostenibilidad agrícola y la adaptación al cambio climático.