En el ámbito de la investigación microbiológica, genética y en laboratorios de diagnóstico, el buffer fosfato es uno de los componentes más fundamentales para los procedimientos experimentales. Este compuesto es crucial para mantener un ambiente controlado en diversos ensayos, permitiendo que las condiciones de acidez y alcalinidad se mantengan estables.
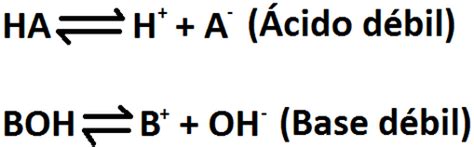
¿Qué es el buffer fosfato?
El buffer fosfato es una solución utilizada principalmente en biología y microbiología para mantener un pH constante. Está compuesto por fosfato de sodio y fosfato de potasio, sales que actúan como amortiguadores. Dado que el pH es un factor determinante para el funcionamiento de enzimas y otras moléculas biológicas, cualquier desviación excesiva puede comprometer la estabilidad de las proteínas, alterar reacciones bioquímicas e incluso afectar la actividad celular.
Importancia del pH en los procesos biológicos
Mantener un pH estable permite que los reactivos biológicos conserven su eficacia. Cuando el pH se desvía, las enzimas pueden desnaturalizarse y las proteínas pierden su conformación tridimensional. El objetivo del buffer fosfato es crear una solución con una capacidad de amortiguación robusta que contrarreste cambios externos, asegurando condiciones óptimas para:
- Cultivos celulares: Vital para la viabilidad de bacterias, hongos o células eucariotas.
- Electroforesis en gel: Mantiene la migración constante de ADN, ARN y proteínas.
- Preparación de muestras para PCR: Garantiza el entorno favorable para la actividad de la polimerasa.
- Análisis de proteínas: Esencial en técnicas como Western blot e inmunoprecipitación.
Procedimiento de preparación de buffer fosfato
Aunque la preparación puede variar según los requerimientos del experimento, el siguiente método describe la creación de una solución estándar. Es fundamental recordar que la preparación debe basarse en cálculos precisos de molaridad (moles/litro).
| Paso | Descripción |
|---|---|
| 1. Selección | Elegir los compuestos base, comúnmente fosfato de sodio (NaH2PO4) y fosfato de sodio dibásico (Na2HPO4). |
| 2. Cálculo | Determinar las concentraciones necesarias según la capacidad de amortiguación requerida. |
| 3. Disolución | Mezclar los reactivos en agua destilada asegurando su completa disolución. |
| 4. Ajuste de pH | Usar una solución ácida (HCl) o básica (NaOH) hasta alcanzar el valor de pH 7.4. |
| 5. Acabado | Filtrar para eliminar impurezas y almacenar en un frasco limpio en condiciones frescas. |
Recomendaciones técnicas
Al preparar soluciones amortiguadoras (también conocidas como tampón o solución reguladora), es vital seguir un rigor metodológico. Un tampón es la mezcla en concentraciones relativamente elevadas de un ácido débil y su base conjugada.
Como consejo aplicable al trabajo de laboratorio: nunca se debe dar por sentado un protocolo sin revisarlo y confirmarlo. Es una buena práctica verificar todos los cálculos y unidades, incluso si han sido realizados anteriormente, para evitar errores de química básica que puedan comprometer los resultados analíticos o la optimización de los métodos.