El agar Mueller-Hinton es un medio de cultivo microbiológico fundamental, ampliamente utilizado en laboratorios clínicos y de investigación para la realización de pruebas de susceptibilidad a antibióticos, comúnmente conocidas como antibiogramas. Su composición y propiedades físicas lo convierten en un entorno ideal para evaluar la eficacia de agentes antimicrobianos contra una variedad de microorganismos, especialmente bacterias patógenas.
Composición y Propiedades del Agar Mueller-Hinton
El agar Mueller-Hinton se caracteriza por ser un medio de cultivo no selectivo y no diferencial. Esto significa que permite el crecimiento de la mayoría de los microorganismos que se inoculan en él, sin discriminar entre especies o proporcionar información sobre sus características metabólicas. Su formulación incluye:
- Extracto de carne bovina y caseína hidrolizada: Estos componentes proporcionan los nutrientes esenciales necesarios para el crecimiento bacteriano, incluyendo aminoácidos, péptidos, vitaminas y minerales.
- Almidón: El almidón presente en la composición actúa como un agente de absorción. Su función principal es neutralizar posibles toxinas liberadas por las bacterias y también absorber el exceso de iones metálicos (como Ca²⁺ y Mg²⁺) que podrían interferir con la acción de ciertos antibióticos, asegurando así la precisión de los resultados.
- Agar: Actúa como agente solidificante, proporcionando la consistencia necesaria para la difusión controlada de los antibióticos. A diferencia de otros medios con mayor proporción de agar, el agar Mueller-Hinton es un agar suelto, lo que facilita una mejor difusión de los antibióticos.
- Agua destilada: Componente base para la disolución de los demás ingredientes.
Una característica crucial del agar Mueller-Hinton es la ausencia de inhibidores que puedan afectar negativamente el crecimiento bacteriano o la acción de los antibióticos. Esta propiedad, junto con su consistencia y composición balanceada, proporciona un entorno óptimo y reproducible para las pruebas de susceptibilidad antimicrobiana.
Desarrollo Histórico
El agar Mueller-Hinton fue desarrollado por John Howard Mueller y Jane Hinton en la Universidad de Harvard. Inicialmente, su propósito era servir como un medio de cultivo para el aislamiento primario del gonococo (Neisseria gonorrhoeae) y el meningococo (Neisseria meningitidis), microorganismos conocidos por sus exigencias nutricionales.

Uso en la Prueba de Susceptibilidad Antimicrobiana (Antibiograma)
El agar Mueller-Hinton es el medio de cultivo de elección para la técnica de Kirby-Bauer, también conocida como el método de difusión en disco. Esta técnica es un procedimiento estándar en laboratorios clínicos para determinar la sensibilidad o resistencia de una bacteria aislada a diversos agentes antimicrobianos.
Preparación del Medio de Cultivo
La preparación del agar Mueller-Hinton implica los siguientes pasos:
- Pesar la cantidad especificada de medio deshidratado (generalmente 37 gramos por litro de agua destilada).
- Disolver el polvo en agua destilada, agitando para facilitar la completa disolución.
- Calentar la mezcla para asegurar la disolución total de los componentes.
- Esterilizar la solución en autoclave a 121 °C durante 15 minutos.
- Después de la esterilización, enfriar el medio en un baño de maría a 50 °C antes de su solidificación.
- Verter el medio en placas de Petri estériles y dejar solidificar.
El medio preparado debe conservarse refrigerado hasta su uso.

Procedimiento de la Prueba de Kirby-Bauer
La técnica de Kirby-Bauer se lleva a cabo de la siguiente manera:
- Inoculación del Medio: Se prepara una suspensión bacteriana a partir de colonias aisladas del microorganismo a estudiar. La turbidez de esta suspensión se ajusta para que coincida con el estándar de 0.5 de la escala de MacFarland.
- Siembra en Superficie: Con un hisopo estéril, se inocula uniformemente toda la superficie del agar Mueller-Hinton, cubriendo de borde a borde. Se gira la placa y se vuelve a sembrar para asegurar una cobertura completa.
- Incubación Inicial: Se deja reposar la placa sembrada durante unos 10 minutos para permitir la absorción del inóculo.
- Colocación de Discos de Antibiótico: Utilizando una pinza estéril, se colocan discos de papel impregnados con diferentes antibióticos sobre la superficie del agar. Se debe mantener una distancia adecuada entre los discos (aproximadamente 24 mm) para evitar la superposición de las zonas de inhibición.
- Incubación: La placa se invierte y se incuba a una temperatura de 35-37 °C en condiciones aerobias durante 16 a 18 horas.
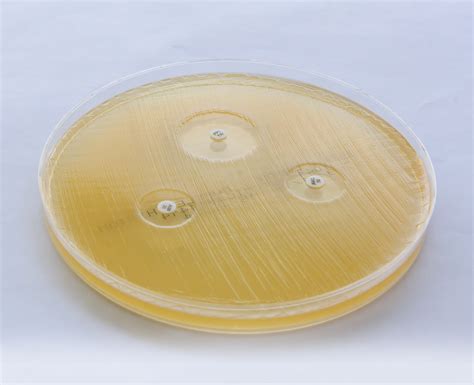
Antibiograma por el método Kirby-Bauer
Interpretación de Resultados
Tras el período de incubación, se observan las zonas de inhibición alrededor de cada disco de antibiótico. Estas zonas son áreas donde el crecimiento bacteriano ha sido impedido por la acción del antibiótico que se ha difundido en el medio.
- Medición de Zonas de Inhibición: El diámetro de cada zona de inhibición se mide en milímetros (mm) utilizando una regla o un dispositivo de medición automatizado.
- Interpretación: Los diámetros de las zonas de inhibición se comparan con tablas estandarizadas (como las proporcionadas por el CLSI - Clinical and Laboratory Standards Institute) para clasificar la bacteria como sensible (S), intermedio (I) o resistente (R) a cada antibiótico.
Consideraciones y Pruebas Adicionales
Aunque la técnica de Kirby-Bauer en agar Mueller-Hinton es un método robusto, existen consideraciones importantes para garantizar la precisión de los resultados:
- Calidad del Agar: La calidad del agar Mueller-Hinton es fundamental. Un medio preparado incorrectamente o contaminado puede llevar a resultados erróneos.
- Conservación de Discos: Los discos de antibióticos deben conservarse adecuadamente para mantener su potencia. Discos mal conservados pueden dar lugar a falsas resistencias.
- Pruebas Específicas: En ciertos casos, se requieren pruebas adicionales o modificaciones para detectar mecanismos de resistencia específicos:
- Detección de BLEE (Betalactamasas de Espectro Extendido): En enterobacterias, se coloca un disco de ácido clavulánico frente a discos de cefalosporinas de 3ª y 4ª generación. Un ensanchamiento en forma de huevo sugiere la producción de BLEE.
- Prueba D-test en Staphylococcus: Para detectar resistencia a clindamicina mediada por el gen erm en estafilococos, se colocan discos de eritromicina o azitromicina frente al disco de clindamicina.
- Detección de AMP C Constitutiva: Se puede evaluar enfrentando un disco de cloxacilina con discos de ceftazidima y cefotaxima, o utilizando un disco de papel de filtro impregnado con ácido fenil bórico.
- Prueba de Imipenem para P. aeruginosa: Este método implica inocular una cepa de Escherichia coli ATCC 25922 en la placa, colocar un disco de imipenem en el centro y luego hacer una estría con la cepa de Pseudomonas aeruginosa sospechosa.