Calentar agua es un proceso físico fundamental que implica la transferencia de energía. Nuestra calculadora de calentamiento de agua permite determinar tanto la cantidad de calor necesaria para elevar la temperatura de una cantidad de H2O, como el tiempo exacto que tardará este proceso en función de la potencia del dispositivo. Comprender los principios termodinámicos es esencial para optimizar el uso de energía en sistemas domésticos e industriales.
Principios físicos del calentamiento de agua
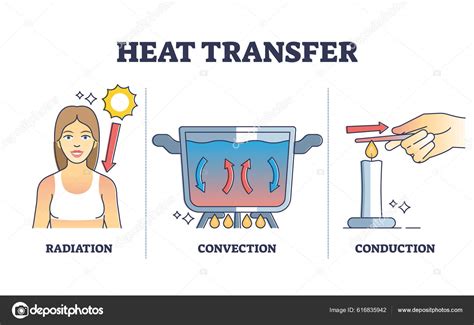
Para calentar agua, es necesario añadir calor, una forma de energía. Al hacerlo, aumenta la energía cinética media de las moléculas y, por tanto, también su temperatura. Existen tres mecanismos principales de transferencia de calor:
- Conducción: Se produce cuando dos objetos están en contacto, permitiendo un flujo de calor del cuerpo caliente al más frío mediante la agitación y colisión de moléculas.
- Convección: Se aplica a los fluidos. Al aumentar la temperatura, el líquido se vuelve menos denso y sube, mientras las partes más frías bajan, creando corrientes circulares que distribuyen el calor.
- Radiación: Se produce a través de ondas electromagnéticas, sin necesidad de un medio material o contacto físico.
Aunque el método de transferencia no influye en la cantidad total de energía necesaria, entender estos principios es vital para cualquier cálculo térmico preciso.
Capacidad calorífica específica y calor latente
Es común confundir términos relacionados con el calor. Definir estas magnitudes es fundamental para realizar cálculos exactos:
| Concepto | Definición | Valor estándar (Agua) |
|---|---|---|
| Capacidad calorífica específica | Energía necesaria para elevar 1 kg de sustancia en 1 Kelvin o 1 °C. | 4190 J/(kg⋅°C) |
| Calor latente de fusión | Energía requerida para cambiar de sólido a líquido a 0 °C. | 334 000 J/kg |
| Calor latente de vaporización | Energía necesaria para pasar de líquido a vapor a 100 °C. | 2 264 705 J/kg |
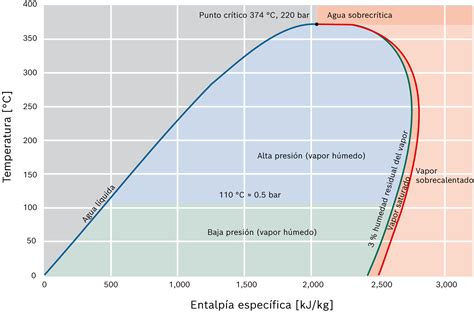
Mientras que el calor sensible aumenta la temperatura sin cambiar la estructura molecular, el calor latente se refiere estrictamente al cambio de fase. El agua posee una gran capacidad calorífica debido a los fuertes enlaces de hidrógeno entre sus moléculas, lo que requiere una cantidad considerable de energía para elevar su temperatura.
Cálculo de la energía y el tiempo de calentamiento
La cantidad de energía (Q) necesaria para cambiar la temperatura depende de la masa (m), el calor específico (c) y la diferencia de temperatura (ΔT): Q = m · c · ΔT. Si el proceso implica un cambio de fase, se debe sumar la energía del calor latente (Q = m · L).
Determinación del tiempo
Si conoces la potencia (P) de tu calentador (ej. un hervidor de 1800 W), puedes calcular el tiempo (t) necesario para alcanzar la temperatura final mediante la fórmula:
t = Q / P
Este cálculo puede ser complejo si se parte de estados iniciales bajos, como hielo a -10 °C. En tales casos, el uso de herramientas automatizadas resulta más eficiente para obtener resultados rápidos.
COMO CALCULAR LA PRESION VAPOR DEL AGUA PARA DIFERENTES TEMPERATURAS✅
Consideraciones sobre la eficiencia y el equilibrio térmico
Al mezclar dos masas de agua a distintas temperaturas, el sistema alcanzará un equilibrio térmico (Teq). La temperatura final se puede derivar de la ecuación de transferencia de calor: Teq = (m · T + m' · T') / (m + m').
Es importante recordar que el entorno actúa como un foco térmico. La pérdida de calor hacia el ambiente sigue una función exponencial: cuanto mayor es la diferencia de temperatura entre el agua y su entorno, más rápido se pierde el calor inicialmente, reduciéndose la velocidad de enfriamiento a medida que se acerca al equilibrio térmico. Por este motivo, para mantener un líquido caliente, la gestión de las condiciones iniciales y el aislamiento del recipiente son factores críticos.