¿Qué es el Punto de Ebullición?
El punto de ebullición de un líquido es un concepto fundamental en la física y la química que representa la temperatura precisa a la que una sustancia líquida pasa al estado gaseoso, es decir, se transforma en vapor. Este valor se refiere al nivel de temperatura en el cual la presión de vapor del líquido iguala la presión ambiental circundante. Al alcanzar esta temperatura, la presión de vapor del líquido llega a ser suficiente para superar la presión atmosférica y permitir que se formen burbujas de vapor dentro de la mayor parte del líquido.
La temperatura de una sustancia o cuerpo es una medida de la energía cinética media de sus moléculas. A medida que calentamos un líquido, las moléculas ganan energía cinética y se mueven más rápidamente. Al llegar al punto de ebullición, la mayoría de las moléculas es capaz de escapar desde todas partes del cuerpo, no solo la superficie. Durante el proceso de ebullición, la temperatura se mantiene constante independientemente de si se añade más energía, aunque esta energía adicional solo produce un aumento en el número de moléculas que escapan del líquido. Este hecho se aprovecha en la definición de la escala de temperatura en grados centígrados.
Factores que Influyen en el Punto de Ebullición
Presión Ambiental
El factor que más afecta el punto de ebullición de un líquido es la presión circundante que lo rodea. Un líquido en un vacío parcial tiene un punto de ebullición más bajo que cuando ese líquido está a la presión atmosférica. Por el contrario, un líquido a alta presión tiene un punto de ebullición más alto que a presión atmosférica.
En sistemas abiertos, la presión suele ser la de la atmósfera misma. Por ejemplo, el agua hierve a 100 °C (212 °F) a nivel del mar, donde la presión atmosférica es de 1 atmósfera (1013.25 hPa o 101.325 kPa). Este punto se denomina punto de ebullición normal o punto de ebullición atmosférico.
A mayor altitud, la presión atmosférica disminuye, lo que causa que el agua hierva a temperaturas más bajas. Por ejemplo, en la cima del Everest, donde la presión atmosférica ronda los 34 kPa, el agua hierve a tan solo 71 °C. El agua hierve a 93.4 °C (200.1 °F) a 1 905 metros (6.250 pies) de altitud. Este efecto tiene implicaciones prácticas, especialmente en la cocina.

El punto de ebullición aumenta con el incremento de la presión hasta el punto crítico, donde las propiedades del gas y del líquido se vuelven indistinguibles, y por encima del cual no existe una fase líquida clara. El punto de ebullición no puede elevarse más allá de este punto crítico. Del mismo modo, el punto de ebullición disminuye con la presión decreciente hasta que se alcanza el punto triple.
Propiedades Moleculares
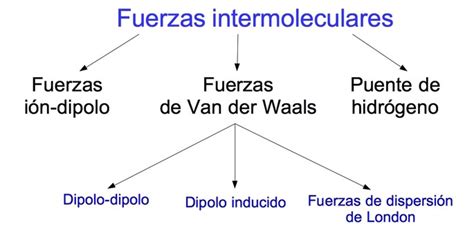
El punto de ebullición también depende de la masa molecular de la sustancia y del tipo de fuerzas intermoleculares que esta posee.
- Masa Molecular: Generalmente, en compuestos con moléculas unidas covalentemente, a medida que aumenta el tamaño de la molécula (o masa molecular), aumenta el punto de ebullición normal.
- Fuerzas Intermoleculares: La polaridad de las moléculas y su capacidad para formar enlaces de hidrógeno afectan significativamente el punto de ebullición. A medida que aumenta la polaridad de las moléculas de un compuesto, su punto de ebullición normal aumenta, siendo iguales otros factores. Los enlaces de hidrógeno, por ejemplo, dificultan que las moléculas abandonen el estado líquido, aumentando así el punto de ebullición. Los ácidos carboxílicos simples se dimerizan formando enlaces de hidrógeno entre las moléculas.
- Tipo de Enlaces: Los compuestos con enlaces iónicos suelen tener puntos de ebullición normales altos, si no se descomponen antes de alcanzar temperaturas tan elevadas. Muchos metales también poseen altos puntos de ebullición.
- Forma Molecular: Un factor menor que afecta los puntos de ebullición es la forma de una molécula.
Un compuesto puro dado tiene solo un punto de ebullición normal, si lo hubiera, y este valor puede servir como una indicación de la volatilidad general de ese compuesto. Cuanto más alto sea el punto de ebullición normal de un compuesto, menos volátil será y viceversa.
Presencia de Impurezas
La presencia de impurezas disueltas (solutos) u otros compuestos miscibles puede afectar las presiones de vapor y, por lo tanto, los puntos de ebullición de las sustancias. Este efecto se conoce como ebulioscopia.
- Impurezas no volátiles: La presencia de impurezas no volátiles, como sales o minerales disueltos, disminuye la fracción molar del componente principal y su volatilidad, elevando el punto de ebullición normal en proporción a la concentración de los solutos. Por ejemplo, añadir sal al agua eleva ligeramente su punto de ebullición.
- Mezclas de componentes volátiles: En mezclas de compuestos miscibles, la presencia de otros componentes volátiles afecta las presiones de vapor y los puntos de ebullición y de rocío de todos los componentes de la mezcla. El punto de rocío es una temperatura a la cual un vapor se condensa en un líquido. Para ilustrar estos efectos, se utiliza comúnmente un diagrama de punto de ebullición.
Ebullición vs. Evaporación
La ebullición se confunde a menudo con la evaporación, aunque son procesos distintos y cruciales en los cambios de estado.
- Evaporación: Es un fenómeno de superficie que ocurre a cualquier temperatura, incluso por debajo del punto de ebullición. Solo las moléculas ubicadas cerca del borde del líquido, que tienen energía suficiente para romper la tensión superficial, escapan a los alrededores como vapor. Es un proceso más lento y requiere que el vapor formado sea removido eficientemente para que continúe.
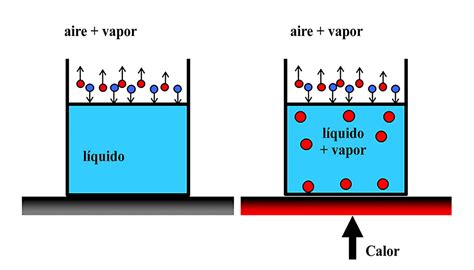
- Ebullición: Es un proceso masivo y volumétrico que ocurre cuando la presión de vapor del líquido es igual a la presión externa, permitiendo la formación de burbujas de vapor dentro de todo el volumen del líquido. La ebullición transcurre de manera intensa, tumultuosa o violenta.
Fenómenos Relacionados con la Ebullición
Supercalentamiento y Nucleación
Un líquido puede calentarse más allá de su punto de ebullición; en ese caso, se le denomina líquido sobrecalentado. En condiciones ultralimpias o en recipientes sin imperfecciones, el agua puede no hervir a 100 °C, sino calentarse uniformemente hasta temperaturas considerablemente más altas (por ejemplo, unos 300 °C), manteniéndose en un estado líquido metaestable.
En un líquido sobrecalentado, una pequeña perturbación puede provocar una ebullición explosiva. Esto ocurre porque la formación de burbujas, un proceso llamado nucleación, requiere una energía de activación. La nucleación puede ser:
- Homogénea: Ocurre espontáneamente en el seno del líquido, por fluctuaciones de densidad o perturbaciones. Requiere un grado de sobrecalentamiento considerable para que se formen núcleos de burbujas con un tamaño mínimo (radio crítico) que no colapsen.
- Heterogénea: Se origina en imperfecciones (cavidades, relieves) en las paredes del recipiente que contiene al líquido. Estas imperfecciones actúan como centros de nucleación, reduciendo significativamente el sobrecalentamiento requerido. La ebullición que observamos en el hogar o laboratorio es típicamente por nucleación heterogénea, con sobrecalentamientos de 5-10 °C por encima del punto de ebullición normal.
agua hirviendo se congela en segundos a 30 grados bajo cero Canadá 🇨🇦
Cuando el líquido adquiere una temperatura cercana al punto de ebullición normal, las burbujas no solo no colapsan, sino que crecen y alcanzan la superficie, generando el proceso masivo y tumultuoso que conocemos como hervor.
Temperatura y Presión de Saturación
La temperatura de saturación es la temperatura para una presión de saturación correspondiente a la que un líquido hierve en su fase de vapor. Se puede decir que el líquido está saturado de energía térmica. Si la presión en un sistema permanece constante (isobárica), un vapor a temperatura de saturación comenzará a condensarse en su fase líquida a medida que se elimina la energía térmica (calor).
De manera análoga, la presión de saturación es la presión para una temperatura de saturación correspondiente a la que un líquido hierve en su fase de vapor. Si la temperatura en un sistema permanece constante (un sistema isotérmico), el vapor a presión y temperatura de saturación comenzará a condensarse en su fase líquida a medida que aumenta la presión del sistema.
Determinación y Medición del Punto de Ebullición
La medición precisa del punto de ebullición es esencial en diversas disciplinas científicas e industriales. Para garantizar resultados precisos, es fundamental estandarizar las condiciones de medición, incluyendo el control de la presión ambiental, el uso de termómetros calibrados y la preparación adecuada de las muestras.
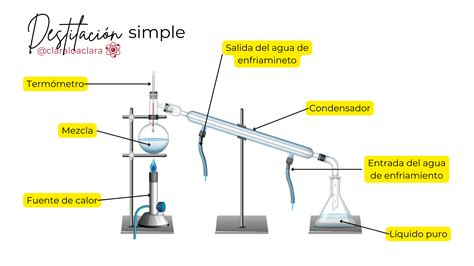
Existen varios métodos para determinar el punto de ebullición:- Destilación: Es una técnica común, especialmente para líquidos puros y mezclas homogéneas. El líquido se calienta hasta la ebullición y los vapores resultantes se condensan y recogen, mientras se mide la temperatura a nivel de vapor.
- Método de Siwoloboff: Un método sencillo y eficaz donde una muestra se calienta en un tubo de ensayo con un capilar sellado. La temperatura a la que dejan de formarse burbujas y el líquido empieza a ascender en el capilar indica el punto de ebullición.
- Calorimetría Diferencial de Barrido (DSC): Un método avanzado para compuestos complejos o sensibles. Se coloca una muestra en un crisol y se calienta a una velocidad controlada. El pico de entalpía detectado en el termograma indica el punto de ebullición.
Aplicaciones Prácticas del Punto de Ebullición
El punto de ebullición es un concepto clave que desempeña un papel crucial en numerosos campos industriales y científicos, desde el procesamiento de alimentos hasta la química analítica.
- Industria Alimentaria: Es crucial para optimizar los procesos de cocción y concentración. Por ejemplo, la cocción a presión en ollas a presión permite alcanzar temperaturas más altas que en condiciones normales, reduciendo el tiempo de cocción y preservando los nutrientes. La destilación se utiliza en la producción de bebidas alcohólicas y aromatizantes. Otro ejemplo es la producción de jarabe de arce, donde el agua se evapora a temperatura controlada para concentrar el azúcar natural.
- Procesos Químicos: Se utiliza para separar y purificar mezclas complejas. La destilación fraccionada, basada en las diferencias en los puntos de ebullición de los componentes, permite recuperar sustancias puras. Es esencial para identificar un producto, ya que cada sustancia tiene un punto de ebullición característico bajo ciertas circunstancias ambientales.
- Industria Farmacéutica y Cosmética: La caracterización de sustancias activas y la formulación de productos se basan en sus puntos de ebullición para garantizar la estabilidad, eficacia y seguridad de compuestos como cremas, lociones y maquillajes. Los disolventes volátiles se seleccionan en función de su punto de ebullición para un secado rápido.
- Refrigeración y Aire Acondicionado: Es esencial para el diseño y funcionamiento de sistemas de refrigeración, ya que sus conductos transportan gases y líquidos que requieren una temperatura de referencia para evitar cambios de estado no deseados.
