La preparación de disoluciones es una habilidad fundamental en el laboratorio químico. Este proceso implica comprender cómo diluir sustancias, gestionar factores de dilución y calcular concentraciones expresadas en diversas unidades, como el porcentaje masa/volumen (m/v).
Conceptos fundamentales de dilución
Una disolución es el producto final resultante de mezclar un soluto con un disolvente. Es crucial identificar correctamente cuál es cada componente para evitar errores en los cálculos. La relación entre dos concentraciones se define mediante el factor de dilución.
- Si una disolución "A" tiene 2 mM y una "B" tiene 2 µM, el factor de dilución para preparar B a partir de A se obtiene comparando ambas concentraciones.
- Para preparar 0,5 litros de una disolución 100 mM de sacarosa a partir de una de 1 M, se debe realizar una dilución 1/10, calculando el volumen exacto que se deberá tomar de la disolución de partida.
- De igual forma, para preparar 200 mL de una disolución 200 mM de NaCl partiendo de una 5 M, se requiere una dilución 1/25.
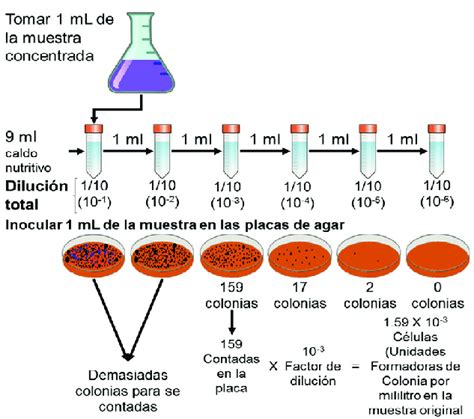
Procedimientos avanzados y diluciones seriadas
En situaciones donde se requiere una reducción drástica de la concentración, se emplean diluciones seriadas (diluciones sucesivas 1/10). Si se desea preparar una serie de muestras de 1 mL, el factor de dilución acumulado determinará la concentración final tras cada paso.
Por ejemplo, en un ensayo con proteínas donde la lectura de absorbancia es demasiado alta, la dilución sucesiva es necesaria:
- Diluciones 1:1 repetidas tres veces.
- Una dilución final de 1/10 para obtener una lectura fiable.
La concentración de la muestra original se obtiene multiplicando la lectura final por el factor de dilución global aplicado.
Cálculo de concentraciones en mezclas
Al preparar una disolución mezclando dos componentes, como glucosa y NaCl, ambos se diluyen en el volumen total final. Un caso práctico sería mezclar 1,0 mL de sacarosa 250 mM con 4,0 mL de NaCl 1,0 M:
| Componente | Volumen inicial | Volumen final | Cálculo | Concentración final |
|---|---|---|---|---|
| Sacarosa | 1,0 mL | 5,0 mL | 250 mM * (1/5) | 50 mM |
Expresiones de concentración: Porcentaje masa/volumen
El porcentaje en masa-volumen (m/v) determina la cantidad de gramos de soluto contenidos en 100 mililitros de solución. Esta unidad física es esencial en la preparación de sueros y soluciones estándar.
Reglas de oro para los cálculos:
- Identificación: Define claramente quién es el soluto, el disolvente y la disolución total.
- Fórmula: Recuerda que en la fórmula del porcentaje se divide entre la cantidad total de disolución, no solo sobre el disolvente.
- Interpretación: Un 10% m/v indica que por cada 100 mL de solución, se requieren 10 g de soluto.
Preparación de una disolución en matraz aforado
Para resolver problemas de este tipo, sigue estos pasos:
- Analiza la incógnita que se presenta (¿% m/v o g de soluto?).
- Determina la cantidad de solución necesaria (por ejemplo, para preparar 120 mL al 35% m/v, utiliza la relación de proporcionalidad directa).